دانلود نمونه سوال رشته شیمی دانشگاه پیام نور
دانلود نمونه سوالات خوردگی فلزات دانشگاه پیام نور
این مطلب در تاریخ: شنبه 17 خرداد 1393 ساعت: 17:59 منتشر شده است
 اميرحسين - واقعا دستتان درد نكند - 1392/2/17
اميرحسين - واقعا دستتان درد نكند - 1392/2/17
 قنبرآبادی - سلام.ممنون فقط لطفا اگه برنامه مقاله را هم داریدلطف کنید.مرسی - 1392/1/9
قنبرآبادی - سلام.ممنون فقط لطفا اگه برنامه مقاله را هم داریدلطف کنید.مرسی - 1392/1/9
 لولو - http://loxblog.ir/images/smilies/smile%20(10).gifhttp://loxb log.ir/images/smilies/smilhthttp://loxblog.ir/images/smiliht tp://loxblog.ir/images/smilieshttp://loxblog.ir/images/smili es/smile%20(26).gif/smile%20(30).gifes/smile%20(3)http://loh ttp://loxblog.ir/images/smilies/smile%20(27).gifxblog.ir/ima ges/smilies/smile%20(14).gif.giftp://loxblog.ir/images/smili eshttp://loxblog.ir/imhttp://loxblog.ir/images/smilies/smile %20(30).gifages/smilies/smile%20(12).gif/smile%20(5).gife%20 (10).gifhttp://loxblog.ir/images/smilies/smile%20(29).gif - 1392/1/5
لولو - http://loxblog.ir/images/smilies/smile%20(10).gifhttp://loxb log.ir/images/smilies/smilhthttp://loxblog.ir/images/smiliht tp://loxblog.ir/images/smilieshttp://loxblog.ir/images/smili es/smile%20(26).gif/smile%20(30).gifes/smile%20(3)http://loh ttp://loxblog.ir/images/smilies/smile%20(27).gifxblog.ir/ima ges/smilies/smile%20(14).gif.giftp://loxblog.ir/images/smili eshttp://loxblog.ir/imhttp://loxblog.ir/images/smilies/smile %20(30).gifages/smilies/smile%20(12).gif/smile%20(5).gife%20 (10).gifhttp://loxblog.ir/images/smilies/smile%20(29).gif - 1392/1/5
 سارا - سلام این ازمایشهای جالب را از کجا اوردین
سارا - سلام این ازمایشهای جالب را از کجا اوردین فلاحتکار - سلام
فلاحتکار - سلام  SARA - مرسی مطلب خوب ومفیدی بود... - 1391/10/19
SARA - مرسی مطلب خوب ومفیدی بود... - 1391/10/19
 7887 - لطفا آزمایش های جالب برای دوم راهنمایی باشند ولی نه آزمایش های گتاب - 1391/10/13
7887 - لطفا آزمایش های جالب برای دوم راهنمایی باشند ولی نه آزمایش های گتاب - 1391/10/13
سایت شیمی کاربردی برای شما دانشجویان و محققین گرانقدر فایل های پاورپوینت آزمایشگاه شیمی آلی 2(کامل به همراه عکس) و کتاب مکانیسم و تئوری در شیمی آلی نوشته ی لری را آماده کرده است.دانلود کنید و لذت ببرید.
دانلود آزمایشگاه شیمی آلی 2 رمز:www.analyte.ir
دانلود کتاب مکانیسم و تئوری در شیمی آلی رمز: alivechem.com
کربن فعال بهعنوان یک جاذب دارای کاربردهای مهم و حیاتی میباشد. این ماده از پیرولیز موادگیاهی حاوی کربن تولید میشود و تحت عملیات فعالسازی قرار میگیرد.
با توجه به نوع موادخام مصرفی، کربنهای فعال دارای اندازه منفذ و شکلهای متفاوت هستند و از طرفی با توجه به اندازه منفذ و توزیع اندازه دارای کاربردهای گسترده و ویژهای میباشند. در این مقاله مراحل تولید کربن فعال و ساختار منفذی انواع کربن فعال مورد بررسی قرار میگیرد.
کربن فعال به گروهی از مواد اطلاق میشود که مساحت سطح داخلی بالا، تخلخل و قابلیت جذب گازها و مایعات شیمیائی را دارند. کربنهای فعال بهعنوان جاذبهای حیاتی در صنایع شناخته شدهاند و کاربردهای گستردهای با توجه به قابلیت جذب گازها و مایعات مزاحم دارند و میتوان از آنها برای تصفیه و پاکسازی و حتی بازیافت موادشیمیائی استفاده نمود. کربنهای فعال بهدلیل ویژگیهای منحصربهفرد و همچنین قیمت پائین در مقایسه با جاذبهای غیرآلی مانند زئولیت از اهمیت ویژهای برخوردار میباشند. کربنهای فعال شده بهدلیل مساحت گسترده آنها، ساختار منفذی، ظرفیت جذب بالا و قابلیت فعالسازی مجدد سطح، یک ماده منحصربهفرد میباشند. کاربرد مهم و قابل اهمیت آنها در جداسازی بو، رنگ، مزههای غیردلخواه از آب در عملیاتهای خانگی و صنعتی، بازیافت حلال، تصفیه هوا بهویژه در رستورانها، صنایع غذائی و شیمیائی میباشد، همچنین با موادغیرآلی بهعنوان کاتالیست نیز استفاده میشوند. در داروسازی نیز برای مبارزه با یک نوع باکتری خاص مورد استفاده قرار میگیرند و بهعنوان جداکننده اسیدهای آروماتیک از حلال در داخل اسیداستیک نیز میتوان از کربن فعال استفاده کرد.کربنهای فعالشده محصولات پیچیدهای میباشند و به تبع طبقهبندی براساس رفتار، مشخصات سطح و روش آمادهسازی آنها مشکل میباشد، هر چند یکسری طبقهبندی براساس مشخصات فیزیکی آنها انجام شده است.
۱. کربن فعال پودری (دارای اندازهای کمتر از ۱۰۰ نامومتو و میانگین قطری بین ۱۵ تا ۲۵ میکرومتر)
۲. کربن فعال گرانولی (دارای اندازهای بزرگتر از کربن فعال شده پودری میباشد)
۳. کربن فعال کروی
۴. کربن تزریق شده
۵. کربن روکش شده با پلیمرها
استاندارد جذب برای کربن فعال مورد استفاده این است که بتواند تا حدود ۲۰% وزنی گاز GB و یا سیانوژن کلراید جذب نماید. اگر کربن فعال تازه باشد و در معرض رطوبت قرار نگرفته باشد خواهد توانست تا ۴۰% وزنی GB جذب نماید. تعداد زیادی از گازهای سمی را میتوان با گذراندن از کربن فعال شده از هوا جدا کرد، این خاصیت برای مواد شیمیائی با وزن مولکولی بالا از قبیل مواد شیمیائی GB مؤثر میباشد، گازهای سبک از قبیل کربن یا سیانوژن کلراید را نمیتوان بهراحتی سایر گازها جدا نمود، منواکسید کربن یکی از موادی است که به سختی میتوان به کمک کربن فعال جذب نمود ولی میتوان با استفاده از تزریق یکسری از موادشیمیائی به کربن فعال، قابلیت جذب اینگونه مواد را در کربن فعال ایجاد نمود و قدرت بازدارندگی کربن فعال را بالا برد. موادیکه بدین منظور میتوان استفاده نمود نمکهای نقره، مس و کرم میباشد.
● مراحل تولید
کربن فعال شده از پیرولیز موادکربنی از قبیل چوب، زغالسنگ و هسته میوهها یا پلیمرهای مصنوعی از قبیل ریون، پلیاکریلونیتریل یا فنولیک حاصل میگردد و در مراحل بعدی تحت عملیات فعالسازی قرار میگیرد. پیرولیز موادکربنی، بدون حضور هوا، باعث تخریب مولکولهای غیرآلی میشود که یک ماده قیری شکل حاوی موادگازدار خواهد بود و در نهایت یک جسم جامد کربنی از آن ایجاد خواهد شد. جسم تولیدشده دارای تعداد زیادی حفرههای بزرگ و دارای سطح ویژهای در حد چندین مترمربع برگرم میباشد.
اتیلن
اتیلن کوچکترین عضو خانوده آلکنها و به فرمول C2H4 میباشد که دو اتم هیدروژن کمتر از آلکان همکربن (اتان) دارد. ما در اینجا به بررسی ساختمان اتیلن میپردازیم تا با ساختار ترکیبات اشباع نشده آشنا شویم. بررسی ساختمان اتیلن به طریق کوانتوم مکانیکی نشان داده است که کربن ، برای اینکه در ساختمان اتیلن شرکت نماید، لازم است که با استفاده از اوربیتالهای 2s و دو اوربیتال 2p خود ، سه اوربیتال هیبریدی یکسان بوجود آورد که این اوربیتالهای هیبریدی ، در یک سطح قرار میگیرند، بنحوی که اتم کربن ، در مرکز یک مثلث قرار گرفته و زوایای بین اوربیتالهای هیبریدی ، 120 درجه تخمین زده شده است.
هرگاه ما چهار اتم هیدروژن و دو اتم کربن sp2 را کنار هم مرتب کنیم، شکلی ایجاد میشود که در آن ، هر اتم کربن در سه پیوند σ (سیگما) شرکت دارد. برای رسیدن به کربن به حالت اکتت ، لازم است که سومین اوربیتال 2p اتمهای کربن همپوشانی کرده ، پیوند ایجاد کنند. این پیوند که از همپوشانی اوربیتالهای p کربن ایجاد میشود، از نظر شکل و انرژی ، با پیوند σ متفاوت میباشد و به پیوند π موسوم است که از دو قسمت تشکیل شده است.
یک ابرالکترونی در بالای سطح مولکول و ابر الکترونی دیگر ، در پایین سطح قرار میگیرد. وقتی این ساختمان میتواند انجام شود که تمام اتمهای شرکت کننده در ساختمان اتیلن در یک سطح قرار گیرند. پس مولکول اتیلن لازم است یک مولکول مسطح باشد. مسطح بودن مولکول اتیلن بوسیله روشهای طیف سنجی و پراش الکترونی مورد تایید قرار گرفته است.
پروپن
پروپن به فرمول C3H6 ، CH3-CH=CH2 ، دومین عضو خانواده آلکنها میباشد که سه اتم کربن با 6 اتم هیدروژن به هم متصل شدهاند.
بوتن
بوتن به فرمول C4H8 عضو بعدی این خانوده است که برای آن ، چند نوع آرایش میتوان در نظر گرفت که در آنها ، چهار اتم کربن با هشت اتم هیدروژن طوری قرار بگیرند که قانون اکتت رعایت شده باشد. بوتن به ظاهر دارای سه ایزومر میباشد، ولی مطالعات تجربی نشان داده است که برای آلکنی به فرمول C4H8 چهار ساختمان فیزیکی کاملا متفاوت وجود دارد.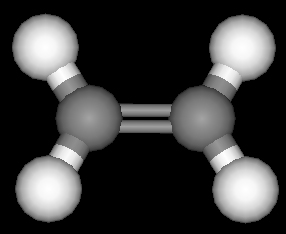
روش آیوپاک برای نامگذاری آلکنها
در روش آیوپاک ، نامگذاری آلکنها با رعایت نکات زیر انجام میشود:
بلندترین زنجیری را که پیوند دوگانه کربن- کربن در آن قرار گرفته باشد، انتخاب میکنیم.
زنجیر اصلی را به نحوی شماره گذاری میکنیم که اولین کربن روی پیوند دوگانه ، کوچکترین شماره را به خود بگیرد. (این روش تنها در مورد مشتقات کربن و هیدروژن صادق است. در نامگذاری الکل های اتیلنی و اسیدها و استرهای اتیلنی و برخی مشتقات دیگر ، اولویت با عوامل الکل ، اسید و استر میباشد.)
شماره کربنهایی را که استخلافها در روی آنها قرار گرفتهاند، مشخص میکنیم.
اگر قرار باشد ایزومرهای هندسی ماده مشخص گردد، در اول نام ماده از پیشوند cis و trans یا E و Z استفاده میکنیم.
خواص فیزیکی آلکنها
بطور کلی ، خواص فیزیکی آلکنها مشابه آلکانهاست. آلکنها در حلالهای غیرقطبی مانند اتر ، کلروفرم و دیکلرو متان محلول ولی در آب نامحلول میباشند و سبکتر از آب نیز میباشند. نقطه جوش آلکنها با افزایش تعداد کربنها افزایش مییابد. بجز آلکنهای کوچک ، نقطه جوش آلکنها به ازای افزایش یک اتم کربن بین 20 تا 30 درجه سانتیگراد افزایش مییابد. همانند آلکانها ، شاخهدار شدن آلکنها موجب کاهش نقطه جوش میشود.
آلکنها اندکی قطبیتر از آلکانها هستند این قطبیت اندک در اثر خصلت الکترون دهی و الکترون گیری گروهها ایجاد میگردد. وقتی روی آلکنها ، گروههای القایی با قدرت بیشتر قرار میگیرد، ممان دو قطبی اندکی افزایش مییابد.


مقاله_-_L_مطالعه_تخريب_حرارتي_در_سنتز_پليلاكتايد_به_روش_پليمر_شدن_.pdf
مقاله_Aspergillus_بررسي_توليد_لواستاتين_از_سويه.pdf
مقاله_GM-CSF_بهينه_سازي_توليد_ترشحی.PDF
مقاله_SCP_بررسی_وضعيت_توليد_و_مصرف.PDF
مقاله_آماده_سازي_و_ويژگي_هاي_لومينسنس_يك_فسفر.pdf
مقاله_اثر_متغيرهاي_فرآيند_پرتودهي_روي_استحكامبه_UHMWPE_PET_كششي_و_.pdf
مقاله_ارائه_روش_موثر_جهت_بازيابي_و_جلوگيري_از_دور_ريز.pdf
مقاله_ارزيابي_عملکرد_باکتريهای_جداسازی_شده_از_مخاز_ن.PDF
مقاله_ارزيابي_نحوه_و_روند_انتشار_آلاينده_هاي_هوا_در.pdf
مقاله_از_آب_و_خاك_آلوده_MTBE_روشهاي_حذف.pdf
مقاله_از_باگاس_نيشكر_(_Biooil_)_توليد_زيست_سوخت.pdf
مقاله_ازمنابع_آب_MTBE_بررسي_حذف_ماده_آلاينده.pdf
مقاله_استفاده_از_تكنولوژي_آنزيم_در_فرآوري_خمير.pdf
مقاله_استفاده_از_روش_افزايش_بيولوژيکي_در_تصفيهپساب_کارخانجات_لبنيا.pdf
مقاله_استفاده_از_شروع_كننده_هاي_دو_عاملي_درپليمريزاسيون_راديكالي.pdf
مقاله_اصلاح_خواص_فيزيكي_و_مكانيكي_سيستم_هاي_برپايه_گل_رس_با_استفاد.pdf
مقاله_اصلاح_شيميايي_ساختار_پليمر_ليفياكريلونيتريل_با_استفاده_از_تر.pdf
مقاله_اصلاح_شيميايي_ساختار_پليمر_ليفياكريلونيتريل_با_استفاده_از_تر.pdf
مقاله_اصلاح_پليمري_كامپوزيت_هاي_بر_پايه_گل_رس.pdf
مقاله_اصلاح_چسبندگي_پلي_يورتان_به_سيليكون_رابر.pdf
مقاله_انتخاب_مدلهاي_سينتيكي_مناسب_براي_بررسي_رشد.pdf
مقاله_اندازه_گيری_غلظت_سلولی_و_تعيين_کيفيت_آن.PDF
مقاله_اولوي_تهاي_بهر_هگيري_از_نانوفناوري.PDF
مقاله_بازده_حذف_بنزن_در_پسابهاي_پتروشيمي_با_فرآيند.pdf
مقاله_بازيابي_آب_كلردار_واحد_كلرآلكالي_شركت_كيميايپتروشيمي_بندراما.pdf
مقاله_بازيابي_پلاتين_از_كاتاليزورهاي_مستعمل_واحد_ريفورمينگ.pdf
مقاله_بر_مورفولوژي_و_(_PVP_)_اثر_پلي_وينيل_پيروليدونغشاء_(_Support.pdf
مقاله_بررسي_آميزه_پلي_وينيل_کلرايد_اکريلونيتريلجهت_تهيه_کاغذ_(PVCN.pdf
مقاله_بررسي_اثر_پارامتر_هاي_مختلف_بر_پليمريزاسيونبه_روش_طراحي_THT_.pdf
مقاله_بررسي_اثرشوك_حرارتي_برروي_پروتئين_تك_ياختهاز_آب_پنير.pdf
مقاله_بررسي_احتمال_تغيير_جرم_مولكولي_متوسط_وزنييك_نمونه_پلي_اكسي_ا.pdf
مقاله_بررسي_ايزومري_شدن_آنزيمي_گلوكز_به_فروكتوز_دريك_جت_راكتور_با_.pdf
مقاله_بررسي_تأثير_فرمولاسيون_و_شرايط_فرآيند.PDF
مقاله_بررسي_تأثير_نسبت_مولي_آلومينيم_به_تيتانيم_درپليمريزاسيون_اتي.pdf
مقاله_بررسي_تأثير_پايدارکننده_ها_و_روان_کننده_ها_برروي_ميزان_فيوژن.pdf
مقاله_بررسي_تاثير_پارامترهاي_موثر_بر_تغيير_رنگ_شربتگلوکز_در_حين_نگ.pdf
مقاله_بررسي_توليد_فيبر_خوراكي_از_تفاله_صنايع.PDF
مقاله_بررسي_جذب_بيولوژيكي_جهت_جداسازي_فلزاتسنگين_از_پسابها-_مو_(1).pdf
مقاله_بررسي_جذب_بيولوژيكي_جهت_جداسازي_فلزاتسنگين_از_پسابها-_مورد_د.pdf
مقاله_بررسي_خواص_فيزيكي_و_مكانيكي_سيستم_گل_رس.pdf
مقاله_بررسي_سينتيك_واكنش_پليمريزاسيون_راديكاليدر_حضور_آغازگر_(MMA).pdf
مقاله_بررسي_عملکرد_وينيل_تري_متوکسي_سيلان_دربهبود_چسبندگي_روکشهاي_.pdf
مقاله_بررسي_عوامل_مؤثر_در_توليد_نانوذرات.pdf
مقاله_بررسي_فرايند_احياي_سولفات_باريم_به_روش_طراحي.pdf
مقاله_بررسي_مقاومت_به_تركزايي_تنشي_محيطي.PDF
مقاله_بررسي_مقاومت_روغني_و_حرارتي_و_سينتيك_نفوذNBRCR_و_آلياژ_CR_،N.pdf
مقاله_بررسي_مكانيزم_انتقال_به_هوا_در_فرايند_حذفبيولوژيكي_اتيل_بنزن.pdf
مقاله_بررسي_ميزان_اتصال_متوكسي_پلي_اتيلن_گليكولفعال_شده_به_سطح_سلو.pdf
مقاله_بررسي_هيدروژل_هاي_حساس_به_دماي_زيستتخريب_پذير_با_پايه_كيتوسا.pdf
مقاله_بررسي_و_آناليز_عناصر_فلزي_سنگين_در_آبهايو_ppb_آشاميدني_مناطق.pdf
مقاله_بررسي_و_بهينه_سازي_اثرات_متقابل_ضريباصطكاك،_چسبندگي_و_چاپ_پذ.pdf
مقاله_بررسي_و_طراحي_سيستم_مناسب_جلوگيري_ازپلي_اتيلن_HD_انتشار_غبار.pdf
مقاله_بررسي_و_مطالعه_حلاليت_دي_اكسيد_كربن_در_حلا_لهاي_آلي_در_دماها.pdf
مقاله_بررسي_وتعيين_خواص_فيزيكي_آب_پنير_جهتاستفاده_در_طراحي_واحدهاي.pdf
مقاله_بررسي_پارامتر_هاي_عملياتي_بر_ثابت_سرعتوسينتيك_خشك_كردن_سيب.pdf
مقاله_بررسي_پتانسيل_اسيدهاي_آمينه_بعنوان_تنها_منبعكربن_و_نيتروژن_د.pdf
مقاله_بررسی_اثر_تغلیظ_اکسیژن_هوا.PDF
مقاله_بررسی_سطح_جذبی_هیدرو_کربنها.PDF
مقاله_بررسی_مکانيزم_انتقال_جرم_در_حين_تشکيل_قطره.PDF
مقاله_بكارگيري_روش_طراحي_آزمايش_تاگوچي_جهتبهينه_سازي_شرايط_رنگبري_.pdf
مقاله_بهينه_سازي_ساختارهاي_ساندويچي_بكار_رفته_در_هوا_فضا.pdf
مقاله_بهينه_سازي_شرايط_عملياتي_سيستم_لجن_فعال_و.pdf
مقاله_بيوتكنولوژي_راهكاري_براي_حذف_تركيبات_مزاحمنيتروژني_از_خوراك_.pdf
مقاله_بيوهيدرومتالورژي_انتخابي_برتر_در_اقتصاد.pdf
مقاله_تأثير_جيبرليك_اسيد_و_سبوس_برنج_بر_توليد_اتانولز_ملاس_و_شربت_.pdf
مقاله_تاثير_آمونياک_بر_گرانولاسيون_لجن_بي_هوازي.pdf
مقاله_تاثير_دما_در_بهينه_سازي_مرحله_تخمير_اكسيداتيودر_فرآيند_توليد.pdf
مقاله_تاثير_روشهاي_مختلف_فرآوري_روي_پايداري_حالتابري_آب_هويج.pdf
مقاله_تاثير_متغيرهاي_عملياتي(شدت_جريان_فازها_وشدت_ضربان)_و_انتقال_.pdf
مقاله_تاثير_مقدار_زيركونيم_روي_عملكرد_كاتاليست_كبالت.pdf
مقاله_تاثير_منبع_کربن_و_نيتروژن_بر_عملکرد_فنوکارئت_کرايزسپريوم_در_.pdf
مقاله_تاثيراستفاده_همزمان_از_دو_آغازگربروزن_مولكولي.pdf
مقاله_تبديل_مستقيم_دی_اکسيد_کربن_دردماي_پائين.PDF
مقاله_تبيين_روشي_جديد_در_فرايند_هيدروليز_متيل.pdf
مقاله_تحليل_رياضي_و_تجربي_بيوراکتور_بستر_ثابت_گلوکزايزومراز_تثبيت_.pdf
مقاله_تخريب_پذير_نمودن_زيست_محيطي_پلي_اتيلن.pdf
مقاله_ترمودینامیک_سطح_محلول_های_پلیمری.PDF
مقاله_تصفيه_آب_نمك_چرخشي_در_كارخانة_توليد_نمكجهت_كاهش_املاح_كلسيم_.pdf
مقاله_تصفيه_الكتروشيميايي_پسابهاي_رنگي_در_محيط_آبي_وبررسي_اثر_ولتا.pdf
مقاله_تعيين_شرايط_بهينه_توليد_بيوسورفكتانت_ها_بهمنظور_استفاده_در_ت.pdf
مقاله_تعيين_ميزان_لاستيك_مقيد_به_عنوان_معياري_ازبا_آلياژ_هاي_N_و_6.pdf
***سنتز p-نیترو آنیلین دانلود
***سنتز p- نیترو استانیلید دانلود
***سنتز استیل سالیسیلیک اسید(آسپرین) دانلود
***سنتز دی بنزال استون با تراکم آلدولی دانلود
سنتز آدي پيك اسيد دانلود

پیوند آروماتیک به یک پیوند آلی گفته میشود که در آن یک حلقه جفت از پیوندهای غیراشباع، جفتهای تکی یا اربیتالهای خالی یک استواری قویتر از استواری جفتسازی تنها را از خود نشان میدهند.
واژه آروماتیک به معنی خوشبو است.
آروماتیکها، دسته وسیعی از ترکیبات را تشکیل میدهند که شامل بنزن و ترکیباتی باشند که از نظر رفتار شیمیایی مشابه بنزن میباشند. برخی از این مواد، حتی به ظاهر شباهتی به بنزن ندارند. برخلاف آلکنها و آلکینها، بنزن و سایر ترکیبات آروماتیک، تمایلی برای انجام واکنشهای افزایش از خود نشان نمیدهند، ولی در واکنشهای جانشینی شرکت میکنند که یکی از صفات شاخص این دسته از مواد میباشد.
اگر گروههای عاملی روی حلقه قرار بگیرند، بر واکنش پذیری حلقه اثر خواهند گذاشت. واکنش پذیری عوامل متصل به حلقه نیز به وسیله بخش آروماتیک تحتتأثیر قرار میگیرد.
مولکولهایی آروماتیک هستند و خصلت آروماتیکی از خود نشان میدهند که تعداد الکترونهای سیستم π آنها، ۲ و ۴ و ۶و ۱۰و… باشد. این ضرورت، قاعده هوکل یا ۴n+۲ نامیده میشود. سپس ترکیباتی که برای آنها n=0, ۱ , ۲ ,… میباشد، آروماتیک خواهند بود.
اگر گروههای عاملی روی حلقه قرار بگیرند، بر واکنش پذیری حلقه اثر خواهند گذاشت. واکنش پذیری عوامل متصل به حلقه نیز به وسیله بخش آروماتیک تحت تأثیر قرار میگیرد.
مجموعه گزارشکارهای آزمایشگاه شیمی آلی 2
کامل به همراه محاسباتوپاسخ سوالات
astanilid.
banzo hydrol.
adepic asid. *
asprin *
capro va diazotitasion. *
kanizaro_aldoli *
sabon. *
siclo oxim va isomerizasion *
لینک دانلود:
پسوردفایل:
نام و نام خانوادگی: کامران مومن زاده
استاد : دکتر قربانی
این آزمایشگاه مربوط به رشته های فنی مهندسی و علوم پایه است.
در این آزمایشگاه آزمایشهای زیر انجام می گیرد:
آزمایشگاه شیمی آلی 1
جلسه 1: اندازه گیری نقطه ذوب
جلسه 2: اندازه گیری نقطه جوش
جلسه 3: کروماتوگرافی
جلسه 4: تبلور مجدد
جلسه 5: استخراج
جلسه 6: آنالیز کیفی ترکیبات آلی ( شناسایی نیتروژن و هالوژن ها)
جلسه 7: تقطیر
جهت دانلود فایل کامل دستور کار روی عنوان آزمایشگاه کلیک نمایید.
استاد :سحر ملکي
نويسنده : کامران مومن زاده
تبلور مجدد
تبلور مجدد یکی از بهترین روش های خالص سازی برای خالص کردن یک جامد است.در این روش اختلاف در حلالیت سبب جدا شدن اجسام از یک دیگر و یا سبب جدا شدن ناخالصی از یک جسم میشود.در تبلور مجدد مولکول ها به تدریج از محلول جدا شده و در ردیف های منظمی به یکدیگر متصل می گردند که به عنوان شبکه شناخته می شوند. در این روش ساختمان بلورین جسم جامد را با انحلال در حلال مناسب بطور کامل از بین می برند و سپس اجازه می دهند تا بلورهای جسم به صورت یک شبکه بلوری مجددا تشکیل شوند.نا خالصی ها معمولا در محلول باقی می مانند.
تبلور مجدد شامل چندین مرحله می باشد:
۱)انتخاب حلال مناسب
۲)انحلال جسم مورد تخلیص در نقطه جوش یا نزدیک آن
۳)صاف کردن محلول داغ برای جدا نمودن ناخالصی های نامحلول
۴)تبلور از محلولی که در حال سرد شدن است
۵)جدا کردن بلورها از محلولی که در آن شناور هستند
۶)شستشوی بلورها برای خارج کردن محلولی که به آنها آغشته است
۷)خشک کردن بلورها
استاد :سحر ملکي
نويسنده : کامران مومن زاده
اندازه گیری نقطه جوش
تعریف نقطه جوش:نقطه جوش دمایی است که در آن دما, فشار بخار جسم مایع با فشار اتمسفر برابر می شود.
نقطه جوش به عوامل زیر بستگی دارد:
۱_ فشار: بین نقطه جوش وفشار ارتباط مستقیم وجود دارد . اگر به تعریف نقطه جوش دقت شود فشار سیستم بالا رود نقطه جوش نیز بالا می رود و بالعکس.
تاثیر فشار بر نقطه جوش:
نقطه جوش یک مایع با تغییر فشار خارجی تغییر میکند. نقطه جوش نرمال یک مایع ، دمایی است که در آن فشار بخار مایع برابر با یک اتمسفر باشد . نقطه جوش داده شده در کتابهای مرجع ، نقاط جوش نرمال میباشند . نقطه جوش یک مایع را میتوان از منحنی فشار بخار آن بدست آورد و آن دمایی است که در آن فشار بخار مایع با فشار وارد بر سطح آن برابری میکند.
نوسانات فشار جو در یک موقعیت جغرافیایی ، نقطه جوش آب را حداکثر تا Cْ ۲ تغییر میدهد . ولی تغییر محل ممکن است باعث تغییرات بیشتر شود ، متوسط فشاری که هواسنج در سطح دریا نشان میدهد یک اتمسفر ، ولی در ارتفاعات بالاتر کمتر از این مقدار است. مثلا در ارتفاع ۵۰۰۰ پایی از سطح دریا متوسط فشاری که فشارسنج نشان میدهد atm 0.836 است و نقطه جوش آب در این فشار Cْ ۹۵٫۱ میباشد.

بنزوئیک اسید، (C7H6O2 (C6H5COOH، یک ترکیب بلوری بی رنگ (سفید دیده میشود) است. بنزوئیک اسید سادهترین کربوکسیلیک اسید آروماتیک نیز میباشد. این ماده یک اسید ضعیف محسوب میشود. از نمکهای آن به عنوان نگهدارندههای غذایی استفاده میشود، همچنین در ساخت بسیاری از ترکیبات آلی دیگر از بنزوئیک اسید استفاده میشود.
تاریخچه
بنزوئیک اسید در قرن شانزدهم میلادی کشف شد. اولین بار شخصی به نام Nostradamus از تقطیر خشک مادهای سنتی به نام gum benzoin بدست آورد. در سال ۱۸۷۵ شخصی به نام Salkowski نیز پی به خواص ضد قارچ بنزوئیک اسید برد.
عنوان آزمایش: تهیه اتیلن
(برای تهیه ی اتیلن روش کارهای مختلفی را می توان در کتابهای شیمی و اینترنت پیدا کرد.اما با وجود یکسان بودن اصل روش،گاهاً دستور کار چندان ساده و ملموس نیست.در این مطلب سعی می کنم ساده ترین روش تهیه اتیلن را که در هر آزمایشگاه شیمی و با ساده ترین امکانات قابل انجام است،بنویسم.)
هدف: تهیه ی اتیلن به روش آزمایشگاهی از اتانول و شناسایی آن با محلول پتاسیم پرمنگنات
مقدمه:
اتیلن ساده ترین آلکن با فرمول C2H4 است.که گازی است بی رنگ و بسیار آتش گیر.
برای تهیه اتیلن روش های مختلفی وجود دارد که از جمله می توان کراکینگ گرمایی اتان(1) و آبگیری از الکل(اتانول) (2)را نام برد.که روش اول صنعتی و روش دوم بیشتر جنبه ی آزمایشگاهی دارد.
(1) CH3-CH3 => CH2=CH2 + H2
(2) CH3-CH2-OH => CH2=CH2 + H2O
اتیلن ( و سایر آلکن ها) با پتاسیم پرمنگنات اکسید می شوند و به این ترتیب رنگ ارغوانی آن را تغییر می دهند.همچنین با آب برم نیز واکنش داده و رنگ قرمز قهوه ای آن را از بین می برند.(روش های شناسایی آلکن ها)
(C2H4 + 2KMnO4+4H2O= 3 C2H4(OH)2 + 2KOH + 2MnO2(s
MnO2 منگنز دی اکسید (قهوه ای رنگ)
KMnO4 پتاسیم پرمنگنات (ارغوانی)
پس تغییر رنگ در طی شناسایی از ارغوانی به قهوه ای خواهد بود.
در صورت استفاده از آب برم تغییر رنگ از قهوه ای یا زرد آب برم به بی رنگ خواهد بود.
C2H4+Br2= C2H4Br2
Br2: برم( قهوه ای یا زرد رنگ)
C2H4Br2 : دی برمو اتیلن (بی رنگ)
در انتها می توان گاز خروجی از لوله ازمایش را با احتیاط آتش زد،که در این صورت گاز اتیلن شعله ور می شود.
از اتیلن در صنعت برای تهیه پلاستیک پلی اتیلن بسیار استفاده می شود.همچنین اتیلن نوعی هورمون گیاهی است که در کشاورزی برای رسیدن میوه هایی که بصورت نارس چیده می شوند(مثل موز) استفاده می شود.
روش کار:
یک تکه پنبه کوچک را به کمک همزن شیشه ای یا یک پیپت در ته یک لوله آزمایش بزرگ قرار می دهیم.چند سی سی اتانول را توسط پیپت روی پنبه ای که ته لوله آزمایش گذاشته ایم،میریزیم،به طوری که کاملاً آغشته به الکل شود.(این آغشته شدن به الکل باید در حدی باشد که موقع افقی کردن لوله آزمایش الکل از پنبه نریزد.) سپس لوله آزمایش را به صورت افقی به میله و پایه ی فلزی وصل می کنیم.به کمک اسپاتول مقداری پودر آلومینیوم اکسید(آلومین) را در وسط لوله آزمایش قرار می دهیم.در لوله آزمایش را با یک درپوش سوراخ دار بسته و لوله ی شیشه ای خمیده ای را به آن وصل می کنیم.(مطابق شکل).
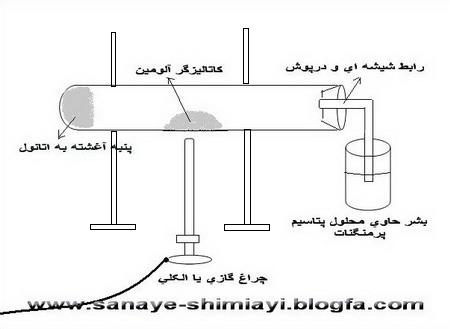
در یک بشر کوچک 50 سی سی تا نصف بشر محلول رقیق پتاسیم پرمنگنات( حدود 0.3% ) می ریزیم.و آن را زیر لوله رابط متصل به لوله آزمایش قرار می دهیم.حرارت را(در زیر قسمتی که آلومین قرار داده ایم) آغاز می کنیم.(گاهی نیز شعله را به سمت ته لوله آزمایش(جایی که پنبه را قرار داده ایم می بریم).اتانول در اثر حرارت و به کمک کاتالیزگر،آب زدایی شده و اتیلن تولید می کند.خروج گاز از لوله ی آزمایش با ایجاد حباب در محلول داخل بشر ثابت می شود.بخشی از این گاز بخار آب است و بخشی از آن گاز اتیلن.
با ورود اتیلن به داخل محلول پتاسیم پرمنگنات رنگ آن قهوه ای یا بی رنگ می شود.( بسته به اینکه محیط اسیدی باشد یا نه).
درست به همین روش می توان به جای پتاسیم پرمنگنات از آب برم نیز برای شناسایی اتیلن استفاده کرد.(بهتر است به جای برم از همن محلول پتاسی پرمنگنات برای ناسایی استفاده کرد چون برم سمی است و باعث سوختگی شدید پوست می شود)
در پایان گزارشکار باید نتیجه ی آزمایش و منابع احتمالی خطا را ذکر کرده و با توجه به مطالب گفته شده در مقدمه و متن روش کار،می توان به سوالات مربوطه پاسخ داد.
زندگینامه ی مندلیف

دیمتری ایوانویچ مندلیف شیمیدان بزرگ روسی در فوریه 1834 در شهر «توبوسك» در سیبری روسیه متولد شد او چهاردهمین فرزند خانواده بود پدرش مدیر مدرسه بود او پدر خود را در کودکی از دست داد. او در مدرسه توپولسک استعداد درخشان خود را در ریاضی و فیزیک نشان داد و عصرها بعد مدرسه در کارگاه شیشه گری به مادرش کمک می کرد مدتی بعد کارگاه شیشه گری آتش گرفت و همه سرمایه شان از دست رفت. دیمیتری برای یافتن شغل بهتر به سن پترزبورگ رفت و در آن جا به تدریس پرداخت در سال 1850 توانست بورس تحصیلی بگیرد و به تحصیل در رشته ریاضی، فیزیک و شیمی بپردازد. او خانواده خود را هم به سن پترزبورگ برد اما متاسفانه مادر و خواهرش به بیماری سل دچار شدند و جان خود را از دست دادند و او تنها شد فقر از یک سو و اندوه از سوی دیگر او را چنان بیمار ساخت که پزشکان تصور کردند او نیز به سل میتلا شده است و به او توصیه نمودند برای معالجه و استراحت به یک محل خوش آب و هوا مسافرت نماید. دیمیتری به جزایر کریمه رفت و مدتی را در آنجا ماند. پس از مدتی او سلامت روحی خود را بازیافت و به سنت پترزبورگ بازگشت...
عنوان آزمایش: خالص سازی مواد به روش استخراج
هدف: استخراج آدیپیک اسید از فاز آبی به فاز آلی(اتر)
تئوری آزمایش:
استخراج روشی است برای جداسازی که در آن جسمی از یک فاز به فاز دیگر منتقل می شود. در بعضی مواقع لازم است برای بازیابی یک ماده آلی از راههایی غیر از تقطیر استفاده شود. یکی از این راهها تماس دادن محلول آبی با یک حلال غیر قابل اختلاط با آب است. اگر حلال مناسب باشد، بیشتر مواد آلی(در اینجا آدیپیک اسید) از لایه آبی به حلال آلی (که با آب امتزاج ناپذیر است) انتقال پیدا میکند.
از نظر کمی پخش یک جسم بین دو حلال غیر قابل امتزاج را بر حسب ضریب پخش K بیان میکنند. به عبارت دیگر ضریب پخش(k) یعنی: نسبت غلظت ماده ی حل شده در حلال اول، به غلظت همان ماده در حلال دوم.
حلالی که برای استخراج انتخاب می شود باید دارای این ویژگیها باشد:
1- با حلالی که دارای ماده مورد نظر است،مخلوط نشود.(سیستم دو فازی تشکیل دهد)
2- K ماده در حلال انتخاب شده بزرگ باشد. (یعنی ماده در حلال دوم بیشتر از حلال اول محلول باشد)
3- حلال نباید ما ماده مورد نظر واکنش دهد.
4- حلال انتخاب شده به آسانی تبخیر شود.
5- حلال نباید ناخالصی ها را استخراج کند.
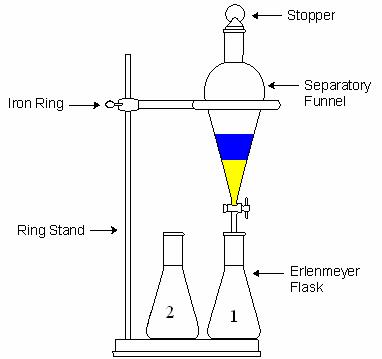
در استخراج مایع-مایع از قیف جدا کننده (دکانتور) استفاده می شود.قیف نباید بیشتر از سه چهارم حجم آن پر شود چون در این صورت امکان هم زدن محلول وجود نخواهد داشت.هدف از تکان دادن و هم زدن این است که سطح تماس دو حلال افزایش یابد و ماده حل شده در حلال اول در مدت زمان کمتری بتواند به حلال دوم برود.(در آن حل شود).هر چند ثانیه یک بار باید قیف را برگرداند(شیر به سمت بالا) و آن را به آرامی باز کرد تا گاز قیف خارج شود.این عمل همیشه باید انجام شود ولی در دو حالت اهمیت بیشتری دارد:
1- وقتی که حلال مورد استفاده دمای جوش پایینی داشته باشد.
2- یک محلول اسیدی با محلولی از سدیم بیکربنات استخراج شود.(در این حالت گاز کربن دی اکسید آزاد می شود)
NaHCO3 + HA = NaA + H2O + CO2
پس از تکان دادن قیف و خارج کردن گازهای آن، قیف جدا کننده را روی گیره ی حلقه ای قرار می دهند و فرصت می دهند تا فازها به خوبی از هم جدا شوند.
استاد : خانم سحر ملکی
نویسنده :
کامران مومن زاده
عنوان:
سنتز استانیلید
هدف:
سنتز استانیلید از آنیلین و استیک انیدرید.
ابزار و مواد لازم:
پیست آب مقطر-ارلن-استوانه مدرج-پیپت-چراغ بونزن-ترازو-کاغذ صافی-قیف شیشه ای
آنیلین-استیک انیدرید-اسید سولفوریک
تئوری آزمایش:
آنیلین
انواع آنیلین
1) تجاری
2) خالص شیمیایی
کاربرد و مصارف
1) بطور وسیع در ساخت رنگهای نساجی و مواد میانی رنگهای نساجی استفاده می شود.
2) در صنایع لاستیک سازی ، از مشتقات آنیلین به عنوان تسریع کننده و تقویت و استحکام لاستیک و ضد اکسید شدن استفاده می شود.
3) در صنایع داروسازی ، آنیلین در ساخت داروهای سولفانیل آمید و عوامل شیرین کننده سنتتیک مصرف می شود.
4) آنیلین همچنین در صنایع انفجاری از اهمیت خاصی برخوردار است و در ساخت ژلاتین و نیتروتولوئن استفاده می شود.
عنوان : گزارش کار تهیه صابون (آزمایش صابونی شدن)
تئوری :
می دانید ساختار یک مولکول صابون به صورت زیر است:
CH3-(CH2)n-COO- +X در صابونهای جامد X یون سدیم و در صابونهای مایع پتاسیم و آمونیوم می باشد.
در تهیه ی صابون ابتدا یون هیدروکسید باز به عنوان نوکلئوفیل (هسته دوست) به کربن گروه کربنیل حمله کرده، پس از خارج شدن یک مولکول الکل، انیون اسید به صورت هیبرید رزونانس فوق، پایدار میگردد.
الکل نقش حلال را دارد. مواد اولیه برای تولید صابون چربی (مولکول آلی و غیر قابل حل در آب) و باز (مانند سود که در آب انحلال پذیر است) می باشند. برای اینکه واکنش بین دو ماده ی اولیه ، یعنی چربی و باز، بهتر صورت گیرد باید از یک حلال استفاده کرد که هر دو ماده ی اولیه را در خود حل نماید. الکل بسیار مفید است زیرا الکل مانند C2H5OH دارای یک سر هیدروکربنی و یک سر قطبی است و می تواند هر دو ماده ی اولیه را در خود حل کرده و درنتیجه واکنش بین ان دو سریعتر و کاملتر انجام گیرد.
| طيف سنجي الكترون براي تجزيه شيميايي(ESCA ) : سلا م دوستان پاورپوينت اين مطلب در اين قسمت گذاشته شده، ... [بیشتر] (194.8 کیلوبایت) | ||||
| الكترو شيمي تجزيه اي : سلام خدمت تمام دوستان شيميستم اين كتاب توي ارشد راحت گي ... [بیشتر] (22.07 مگابایت) | ||||
| اطلاعاتي در مورد SPE : تقديم به همه دوستان شيميستم ، اگر بدردتون خورد بدردتون ... [بیشتر] (161.7 کیلوبایت) | ||||
| اسلاید آموزش مبحث هیبریداسیون : هیبریداسیون یکی از مباحث نظریه ی vespr است که آشنایی با ان ... [بیشتر] (1.05 مگابایت) | ||||
| گرافن باریکترین ضد زنگ : این text درباره گرافن است (11.6 کیلوبایت) | ||||
| فزایش استحکام گرافن با تا زدن آن : این text در مورد گرافن است (11.8 کیلوبایت) | ||||
| آموزش محلول سازی : این text در مورد طریقه محلول سازیست (173.9 کیلوبایت) | ||||
| ساخت باطری با گرافن : این text در مورد باطری جدید از گرافن است (12.3 کیلوبایت) | ||||
| راهنمای شیمی آلی ولهارد جلد سوم (فصل 26) : راهنمای شیمی آلی ولهارد جلد سوم (فصل 26: آمینواسیدها، پپ� ... [بیشتر] (2.42 مگابایت) | ||||
| راهنمای شیمی آلی ولهارد جلد سوم (فصل 25) : راهنمای شیمی آلی ولهارد جلد سوم (فصل 25: هترواتمها در ترک ... [بیشتر] (1.82 مگابایت) | ||||
| راهنمای شیمی آلی ولهارد جلد سوم (فصل 24) : راهنمای شیمی آلی ولهارد جلد سوم (فصل 24: کربوهیدراتها) تش ... [بیشتر] (2.22 مگابایت) | ||||
| راهنمای شیمی آلی ولهارد جلد سوم (فصل 23) : راهنمای شیمی آلی ولهارد جلد سوم (فصل 23: ترکیبهای دی کربو ... [بیشتر] (1.66 مگابایت) | ||||
| راهنمای شیمی آلی ولهارد جلد سوم (فصل 22) : راهنمای شیمی آلی ولهارد جلد سوم (فصل 22: شیمی بنزن استخ� ... [بیشتر] (2.34 مگابایت) | ||||
| راهنمای شیمی آلی ولهارد جلد سوم (فصل 21) : راهنمای شیمی آلی ولهارد جلد سوم (فصل 21: : آمینها و مشتقات ... [بیشتر] (2.67 مگابایت) | ||||
| راهنمای شیمی آلی ولهارد جلد سوم (فصل 20) : راهنمای شیمی آلی ولهارد جلد سوم (فصل 20: مشتقات کربو کسیل ... [بیشتر] (2.57 مگابایت) |
| راهنمای شیمی آلی ولهارد جلد سوم (فصل 19) : راهنمای شیمی آلی ولهارد جلد سوم (فصل 19: کربو کسیلیک اسید ... [بیشتر] (2.21 مگابایت) | ||||
| آمونیاک : 17 صحفه (126.5 کیلوبایت) | ||||
| افزایش حجم آب هنگام انجماد : 1 صحفه (16.4 کیلوبایت) | ||||
| آشنایی با علائم هشدار دهنده در آزمایشگاه شیمی : 1 صحفه (371.0 کیلوبایت) | ||||
| Flame Ionization Detector - FID : این مقاله در مورد "دتکتور های FID " هست که در دستگاه های تج ... [بیشتر] (1.12 مگابایت) | ||||
| مول : 1 صحفه (13.7 کیلوبایت) | ||||
| پلیمرها : سلام این کتاب برای افرادی که در صنایع پلیمری مشغول به ف ... [بیشتر] (3.94 مگابایت) | ||||
| Food Lipids Chemistry, Nutrition, and Biotechnolog : 5.7MB زبان اصلی 1016ص (5.70 مگابایت) | ||||
| inorganic chemistry : زبان اصلی (3.42 مگابایت) | ||||
| آمونیاک : آمونیاک محرک خسارت نوری فتوسیستم 2 در حضور باکتری Cyanobacte ... [بیشتر] (126.5 کیلوبایت) | ||||
 |
شیمی سال دوم دبیرستان : کتاب شیمی دوم دبیرستان در سال 1340 (1.40 مگابایت) | |||
| Synthetic Methods Catalysis : (1.58 مگابایت) | ||||
| بررسي روش استخراج با حلال براي تصفيه فسفريك اسيد ص : -;{@ (218.1 کیلوبایت) | ||||
| Inorganic chemistry : -;{@ (4.89 مگابایت) | ||||
| لغت نامه ي شيمي : اين لغت نامه انگليسي به انگليسي است (2.88 مگابایت) |
 2) دانلود خلاصه درس شیمی آلی 1 - شیمی آلی و آزمایشگاه (در قالب PowerPoint)
2) دانلود خلاصه درس شیمی آلی 1 - شیمی آلی و آزمایشگاه (در قالب PowerPoint)
 3) دانلود خلاصه درس شیمی آلی 1 - شیمی آلی و آزمایشگاه (در قالب PowerPoint)
3) دانلود خلاصه درس شیمی آلی 1 - شیمی آلی و آزمایشگاه (در قالب PowerPoint)
 4) دانلود خلاصه درس شیمی آلی 1 - شیمی آلی و آزمایشگاه (در قالب PowerPoint)
4) دانلود خلاصه درس شیمی آلی 1 - شیمی آلی و آزمایشگاه (در قالب PowerPoint)
در شيمي پيوند آروماتيک به يک پيوند آلي گفته ميشود که در آن يک حلقه جفت از پيوندهاي غيراشباع، جفتهاي تکي يا اربيتالهاي خالي يک استواري قويتر از استواري جفتسازي تنها را از خود نشان ميدهند.واژه آروماتيک به معني خوشبو است.
آروماتيکها، دسته وسيعي از ترکيبات را تشکيل ميدهند که شامل بنزن و ترکيباتي باشند که از نظر رفتار شيميايي مشابه بنزن ميباشند. برخي از اين مواد، حتي بهظاهر شباهتي به بنزن ندارند. برخلاف آلکنها و آلکينها، بنزن و ساير ترکيبات آروماتيک، تمايلي براي انجام واکنشهاي افزايش از خود نشان نميدهند، ولي در واکنشهاي جانشيني شرکت ميکنند که يکي از صفات شاخص اين دسته از مواد ميباشد.

مشتقات بنزن با فشار بالا و نقطه جوش پايين هستند که با افزايش وزن مولکولي افزايش مي يابد. اين حلال داراي دانسيته بخار بالا هستند. بيشتر اين ترکيبات به عنوان مواد شميايي اوليه يا واسطه در ترکيبات ديگر بکار مي روند. حلالهاي الي همچنين در هزاران صنعت وشغل مثل :توليد رنگ ،رزين ومواد دارويي ،چاپ ، سريش و چسبها و ساخت لاستيک و… بکار مي رود.
ترکيبات اروماتيک معمول استفاده شده شامل تولوئن ،بنزن ،زايلن ،استيرن ،اتيل بنزن ،مونوکلروبنزن (MCB ) وتري متيل بنزن مي باشد. بيشتر حلالهاي اروماتيک تجاري نقطه جوشي دارند که خيلي کمتر از صفر درجه و بشتر از 200 درجه سانتيگراد نمي باشد.اگر نقطه جوش يک حلال خيلي بالاوفشار بخار آن خيلي کم باشد جداسازي حلال از موادي که براي حل کردن استفاده مي شود بسيار دشوار خواهد بود.بنابراين بسياري از حلالهاي الي در دماي اتاق مايع هستند.
حلالهاي الي بوسيله خصوصيت غير قطبي وحلاليت بالا در چربي توصيف مي شوند. اين حلالها به فراواني در مخلوطهايي در محيطهاي شغلي مثل ترکيبات تولوئن ، بنزن ، استيرن ،اتيل بنزن ، تري متيل بنزن و زايلن استفاده شده است. نفتالن ، اگر چه يک ترکيب اروماتيک است حلال نيست ، جامدي کريستالي ، سفيد رنگ دافع بيد و با فراريت بالا مي باشد. حلالهاي اروماتيک به اساني از تصفيه نفت خام و زغال مشتق مي شود وقتي زغال در فقدان هوا گرم مي شود به ترکيبات فراري شامل گاز زغال وقطران زغال شکسته مي شود. باقيمانده اين پروسه کک ناميده مي شود. تقطير قطران زغال منجر به توليد ترکيباتي مثل تولوئن ،بنزن ،زايلن ، فنول ها ، کروزول ، نفتالن مي شود.ترکيبات اروماتيک همچنين مي تواند توسط فرايند هاي کاتاليکي که در ان هيدروکربن هاي اليفاتيک در دماهاي بالا وفشار بالا براي دهيدروژنه کردن ترکيبات وشکل گيري ساختارهاي حلقوي هيدروکربن هاي اروماتيک بکار مي رود ايجاد مي شوند.
◄ فاکتورهاي دخيل در سميت حلالها:
تماس با حلالهاي اروماتيک ار طريق تماس با بخار يا مايع انها رخ مي دهد راههاي اصلي جذب راه تنفسي وپوستي است. سميت حلالها به ترکيب فيزيوشميايي انها ، سميت ذاتي ، متابوليت ها و داروهاي کلينيکي بستگي دارد. براي حلالهايي مثل بنزن و استيرن متابوليت ها سموم اصلي هستند.
فاکتورهاي سميت مي تواند بصورت زير خلاصه شود:
1. ماهيت سمي ترکيب اصلي
2. طبيعت سمي متابوليت ها
3. بافت ها وارگان هاي هدف
4. مداخله با ديگر داروها يا حلالها
5. اثر بيماريهاي قلبي
6. تماس (دوز ،مدت ، شدت )
7. خاصيت فيزيکو شميايي حلال (فشار بخار ، دانسيته بخار ، واکنش پذيري )
8. راههاي تماس (تنفسي ، پوستي ، GI )
کربوکسیلیک اسیدها دستهای از ترکیبهای آلی هستند که یک یا چند گروه عاملی کربوکسیل«COOH-» در آنها یافت میشود.متانوییک اسید سادهترین و اتانوییک اسید آشناترین آن هاست. کربوکسیلیک اسیدهای سبک (حداکثر تا چهار اتمکربن)به خوبی در آب حل میشودولی با افزایش طول زنجیره کربنی از انحلال پذیری آنها در آب کم میشودبه طوری که بسیاری از آنها در عمل در آب نا محلولند. کربوکسیلیک اسیدها اسیدهای ضعیفی هستند و بر اثر حل شدن در آب تعدادی از مولکولهای آنها پروتون اسیدی خود را به مولکولهای آب میدهندو به سرعت به حالت تعادل میرسند.
این اسیدها یک، دو یا چند عاملی هستند که به اسیدهای آلی چند عاملی پلی الکترولیک میگویند.
| نام | نام دیگر | فرمول شیمیایی | pKa |
|---|---|---|---|
| فرمیک اسید | جوهر مورچه | HCO2H | ۳.۷۷ |
| اتانوییک اسید | استیک اسید-سرکه | CH3COOH | ۴.۷۶ |
| پروپانوییک اسید | - | C2H5COOH | |
| بوتانوییک اسید | بوتریک اسید | C3H7COOH | |
| دیاتانوییک اسید | اگزالیک اسید | HO2CCO2H | ۱.۲۷ |
| سوکسینیک اسید | - | ||
| آبیتیک اسید | - | ||
| بنزوییک اسید | - | C6H5CO2H |
در این روش از نامی که از دیر باز برای آن به کارمی رفته بهره میجویند. مانند:استیک اسید.
این روش امروزه با وجود شمار فراوان ترکیبهای آلی کم کاربرد تر شده ولی هنوز در کاربردهای تجاری از همین روش بهره میگیرند.
آلکینها هیدروکربنهایی هستند که دست کم یک پیوند سهگانه بین دو اتم کربن دارند. از آنجا که کوچکترین آلکین که نام آیوپاک آن اتین (C۲H۲) است، پیشتر به نام استیلن شناخته میشده است؛ آلکینها به نام استیلنها یا گروه اسیتیلنی نیز نامیده میشوند.
روش جامع برای نامگذاری آلکینها روش آیوپاک(IUPAC) است و اصول آن، مشابه نامگذاری آلکنهاست و با رعایت نکات زیر انجام میشود:
خواص فیزیکی آلکینها، مشابه آلکنهای هم کربن است. آلکینها، ترکیباتی با قطبیت بیشتر هستند که در حلالهای با قطبیت کمتر مثل تتراکلرید کربن، بنزن و اترها بخوبی حل میشوند، ولی در آب نامحلولند. همانند سایر هیدروکربنها سبکتر از آب هستند. بررسی و مقایسه نقطه ذوب و نقطه جوش این مواد نشان میدهد که با افزایش تعداد کربن نقطه جوش افزایش مییابد و با شاخهدار شدن کاهش مییابد.
به طور کلی دو روش زیر برای فرآوری آلکینها به کار میرود:
آلکنها، هیدروکربنهایی هستند که یک پیوند دوگانه کربن – کربن (C=C) دارند. آلکنها سیر نشده هستند، یعنی میتوانند هیدروژن بگیرند و سیر شوند.
برای نامگذاری آنها از دستور زیر استفاده میشود:
تعداد اتمهای کربن (به عدد یونانی) + پسوند (ان)
آمید را در شیمی میتوان یکی از دو نوع ترکیب شیمیایی زیر دانست:
آمیدها پایدارترین نوع از گروه عاملی کربونیل هستند.

بسیاری از شیمیدانان انگلیسیزبان برای ایجاد دگرسانی میان این دو نوع ترکیب، از تلفظ {{|ə'mɪd}} برای اشاره به این ترکیب به عنوان یک گروه عاملی کربونیل و از تلفظ ['æmɑɪd] برای اشاره به آن به عنوان آنیون نیتروژن بهره میگیرند. این در حالی است که شماری از شیمیدانان نیز فرقی میان این دو نگذاشته و در هر دو کاربرد آن را ['æmɪd] تلفظ میکنند.
اگر در بنیان آمیدها جایِ کربنی که با اکسیژن پیوند دوگانه دارد گوگرد قرار دهیم گروهی به نام سولفوآمید خواهیمداشت.
آمیدهای حلقهای را لاکتوم مینامند.
اتر نامی است که به ترکیبهای شیمیایی که گروه اتری دارند گفته میشود. این گروه یک اکسیژن است که از دو سو به دو گروه آلکیل پیوند دارد.
روش معمولی نامگذاری اترها به شکل آلکوکسی آلکان است. برای نمونه:(اتوکسیاتان، CH۳-CH۲-O-CH۲-CH۳). هر چند که روش کمکاربردتری نیز برای نامگذاری اترها هست که در آن نخست نام دو گروه آلکیلی که با اکسیژن پیوند دارند آمده و سپس نام اتر میآید. اتر نامبرده در روش دوم دیاتیل اتر نامگذاری میشود.
اترها بسته به گروه کربنی که به اکسیژن آنها پیوند داشته باشد در این سه گروه جای میگیرند. در اینجا از هر نوع یک نمونه آورده شدهاست. یک اتر نوع اول: دیاتیل اترCH۳-CH۲-O-CH۲-CH۳. یکاتر نوع دوم:دیایزوپروپیل اتر (CH۳)۲CH-O-CH(CH۳)۲ و یک اتر نوع سوم: دیترسیوبوتیل اتر (CH۳)۳C-O-C(CH۳)۳.
دیمتیل اتر، یک اتر نوع اول، نوع دوم، نوع سوم
یک کتون یک گروه عاملی است که با یک گروه کربونیل که با دو اتم کربن دیگر پیوند دارد؛ شناخته میشود. یک کتون را میتوان با فرمول زیر بیان کرد.
اتم کربن که با دو اتم کربن پیوند دارد آن را از گروههای عاملی کربوکسیلیک اسیدها، آلدهیدها، استرها، آمیدها و دیگر ترکیبهای اکسیژندار جدا میکند. پیوند دوگانهٔ گروه کربونیل نیز کتونها را از الکلها و اترها باز میشناساند.
به کربنی که به کربن گروه کربونیل چسبیده کربن آلفا و به هیدروژنی که به این کربن چسبیده هیدروژن آلفا گویند. در حضور یک کاتالیزور اسیدی کتون به keto-enol tautomerism مربوط میشود. واکنش با یک پایه قوی انول متناظر را نتیجه میدهد
برای دیگر کاربردها، آمین (ابهامزدایی) را ببینید.
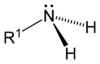
| آمین نوع یک | آمین نوع دو | آمین نوع سه |
|---|---|---|
 |
 |
 |
آمینها(به انگلیسی: Amines)) ترکیبات آلی هستند که جزو بازها به شمار رفته و یک اتم نیتروژن مرکزی و یک یا دو یا سه گروه آلکیل متصل به آن هستند که به ترتیب آمین نوع یک، آمین نوع دو و آمین نوع سه نامگذاری میشوند آمینها معمولا از آمونیاک استخراج میشوند که جای هیدروژنها گروه آلکیلی قرار میگیرند. خاصیت بازی آمین نوع دوم از بقیه بیشتر بوده و این گروه با تاثیر روی سیستم عصبی انسان کاربردهای گستردهای پیدا کردهاند و بعضی از پیکهای عصبی انسان مانند آدرنالین آمین اند و بعضی از جلوگیری کنندهها مانند مرفین نیز در گروه آمینها قرار میگیرند. از دیگر ترکیبات آمین میتوان به کدیین، افندرین، اشاره کرد. از دیگر آمینهای مهم آمینواسیدها نیز هستند.
آمینهای کوچک سمیاند و بعضی از آنها خاصیت خورندگی پوست انسان را دارند و آمینهای بزرگ معمولا از لحاظ زیستشناسی بسیار فعالند.
آلدهید ترکیبی آلی است که یک گروه کربونیل در یک سر خود دارد. این گروه عاملی دارای کربنی است که از یک سو با پیوند دوگانه به اکسیژن و از سوی دیگر یک اتم هیدروژن پیوند دارد. فرمول شیمیایی این بخش از ماده را (-CHO) مینویسند.
گروه عاملی، در شیمی آلی، به گروههای معینی از اتمهای یک مولکول گفته میشود که در واکنشهای شیمیایی ویژه آن مولکول شرکت میکنند. گروههای عاملی یکسان در یک مولکول به واکنش شیمیایی یکسان در آن مولکول میانجامند.
برای نمونه گروه عاملی آلدهید میتواند واکنش کاهش و اکسایش بدهد.
در زیر لیستی از گروههای عامل متداول است. در فرمول، نمادهای R و 'R که معمولاً به معنی هیدروژن و یا زنجیرههای هیدروکربن با هر طول ممکن است، ولی برخی اوقات ممکن است به هر گروه از اتمهای برگردد.
گروههای عاملی که بر اساس تعداد و طرز قرار گیری پیوندهای پی تفاوت شیمیایی پیدا میکند. همهٔ موارد زیر شامل پیوندهای C-H است اما هریک تفاوتهایی در نوع واکنش پذیری دارد.
| رده شیمیایی | گروه | فرمول | فرمول ساختاری | پیشوند | پسوند | مثال |
|---|---|---|---|---|---|---|
| آلکان | آلکیل | RH | آلکیل- | -ane |  اتان |
|
| آلکن | آلکنیل | R۲C=CR۲ |  |
آلکنیل- | -ene | 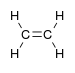 اتیلن (اتن) |
| آلکین | آلکینیل | RC≡CR' | آلکینیل- | -yne | استیلن (اتین) |
|
| مشتقات بنزن | فنیل | RC۶H۵ RPh |
فنیل- | -بنزن | 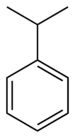 کومن (۲-فنیل پروپان) |
|
| مشتقات تولوئن | بنزیل | RCH۲C۶H۵ RBn |
بنزیل- | ۱-تولوئن | بنزیل بورومید (۱-بروموتولوئن) |
همچنین تعداد زیادی شاخهیا آلکانهای حلقوی هستندکه نامهای مخصوص دارند برای مثال ترت-بوتیل، بورنیل، سیکلوهگزیل و غیره.
گلیسرول، الکل سه عاملی است که به هر نسبتی در آب حل میشود؛ ولی در اتانول و دیگر حلالهای آلی بسیار کم محلول است. گلیسرول شیرین، شفاف، بیرنگ و بیبو است و در حضور گرما و مواد آبگیر (مانند HSO4K)، آب از دست داده به آلدئید دود کننده با بوی بد که مخاط را به شدت آزار میدهد تبدیل میشود. ایجاد آکرولئین با این مشخصات راهی برای تشخیص گلیسرول است.
گلیسرول در طبیعت بیشتر به صورت ترکیب با اسیدهای چرب است که چربی را میسازد. برای نمونه یک مولکول گلیسرول با ۱ یا ۳ اسید چرب مونوگلیسرید یا تریگلیسرید را می سازد؛ مانند روغن نباتی و ... .
اتانول یا الکل اتیلیک یا اتیل الکل با فرمول C۲H۵OH ترکیب شیمیائی با بوی خاص و آتشگیری است که در نوشیدنیهای الکلی وجود دارد. این الکل همان مادهای است که خاصیت مست کنندگی دارد و در نوشیدنیهای الکلی با درصدهای مختلف پیدا میشود. علاوه بر این در صنایع مختلف کاربرد فراوان دارند. این کاربردها در عطرها و ادکلنها و همچنین در وانیل و همچنین به عنوان سوخت در برخی ماشینهای جدید میباشد. برای استفاده از این الکل در صنایع عطر سازی استفاده میکنند.
مخمر آبجو ، قارچی است که با جوانهزدن تکثیر میشود، اگر این قارچ در مجاور یک ماده قندیتخمیر شود، موادی از خود خارج میکند که خاصیت آنزیمی داشته و موجب دگرگونی قند میشود. در بین قندها ، گلوکز به فرمول C۶H۱۲O۶ است که در انگور وجود دارد که پس از تخمیر باعث ایجاد الکل میشود.

در این پست اسلایدهای پاورپوینت مرتبط با آموزش شیمی را قرار میدهیم و قصد داریم آن را به مرور زمان به روز کنیم. ضمن این که تشکر خود را از عزیزانی که این پاورپوینتها را تهیه نموده و به اشتراگ گذاشتهاند، اعلام مینمائیم.
باز تعریف آنتروپی از دیدگاه ماکروسکوپی و مولکولی با رویکرد آموزشی (همراه با ارزیابی کتاب شیمی ۳ در رابطه با آنتروپی و قانون دوم)
تهیه کننده: دکتر غلامعباس پارسافر (دانشگاه صنعتی شریف)
۱٫۵۱MB
مدل الکترون نقطه ای و ساختار لوئیس
تهیه کننده: مجید معین السادات (با تشکر از آقای فرشاد میرزائی ولدی بخاطر معرفی)
۷۱۷KB
ماده و ساختار آن
تهیه کننده: منصور رحیمی (از شهر بم)
۱٫۴۴MB
استفاده از آنالوگ در آموزش شیمی
دبیرخانه راهبری درس شیمی- تهران
۹۹۵KB
اصل آفبا و آرایش الکترونی اتمها
تهیه کننده: عبدالکریم فاضلی (سرگروه شیمی استان کهگیلویه و بویر احمد)
۱٫۵MB
آموزش شیمی ۲: بخش اولبخش دومبخش سومبخش چهارمبخش پنجم
تهیه کننده: آقایان همایونی و توکلی (گروه شیمی استان فارس)
۱۱MB
پیوند قطبی
تهیه کننده: هاجر علیپورنیا (گروه شیمی شهرستان نقده)
۳۰۰KB
انتروپی
تهیه کننده: شایان نصرالهی (دبیر شیمی شهرستان نوشهـر)
۷۰۰KB
خواص کولیگاتیو محلولها
تهیه کننده: شایان نصرالهی (دبیر شیمی شهرستان نوشهـر)
۱٫۱MB
فنولها ترکيبات اسيدي هستند که قدرت اسيدي آنها از کربوکسيليک اسيدها کمتر است اين امر در مورد فنولهايي که داراي استخلافهاي نيترو هستند صدق نمي کند. برخی از آزمايشهايي که در شناسايي فنولها مورد استفاده قرار مي گيرد در زیر امده است.
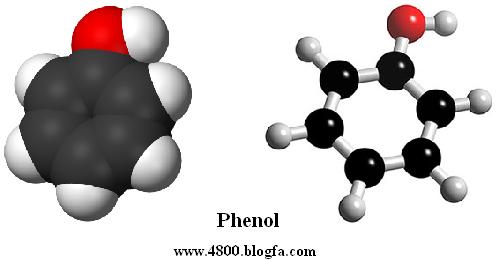
1- محلول سديم هيدروکسيدانحلال پذيري فنولها در محلول سيدم هيدروکسيد، در مورد فنولهايي که امکان مزدوج شدگي در باز مزدوج (آنيون فنولات) آنها زياد است، با رنگي شدن محلول همراه است. براي مشاهده رنگ، بايد مقدار کمي از فنول را در محلول سديم هيدروکسيد 10% حل نمود. انحلال بعضي فنولها با رنگي شدن همراه نيست. و تعدادي از آنها نيز در محلول سديم هيدروکسيد نامحلول هستند و بصورت رسوب مي باشند.
2- فريک کلريد فنولهاي محلول در آب
چند قطره محلول آبي فريک کلريد 5/2% به يک ميلي ليتر محلول آبي و رقيق فنول ( حدود 3-1% وزني ) اضافه نماييد. در مورد بيشتر فنولها رنگ قرمز تند، آبي، ارغواني يا سبز ظاهر مي شد. بعضي رنگها بصورت گذرا هستند و براي مشاهده رنگ بايد محلول خوب همزده شود و مخلوط گرد رنگي شدن معمولا فوري است. اما بايد توجه داشت که رنگ محلول براي زمان زيادي پايدار نيست.
فنولهاي نامحلول در آب بسياري از فنولها با روشي که پيش از اين ذکر شد و به آزمايش فريک کلريد پاسخ مثبت نمي دهند و بايد آزمايش را بدين ترتيب انجام داد که 20 ميلي گرم از فنول جامد يا يک قطره فنول مايع را در يک ميلي ليتر کلروفرم حل يا به حالت تعليق درآورد و سپس يک قطره پيريدين و سه تا پنج قطره از محلول 1 % فريک کلريد ( حجم/ وزن ) در کلروفرم به آن اضافه نماييد.
3- برم / آب
محلول آبي 1 % از مجهول تهيه نماييد سپس به آن قطره قطره محلول آب برم اشباع شده اضافه نماييد و هر بار تکان دهيد تا رنگ زايل شود. تشکيل رسوب به دليل توليد محصوص استخلاف شده است که همزمان با از بين رفتن رنگ برم است به عنوان نتيجه مثبت براي اين آزمايش تلقي مي شود.
تهيه مشتق ها
مشتقات فنولها اورتانها هستند که از واکنش فنول با ايزوسيانات توليد مي شود. مشتق هاي ديگر براي فنولها 3 و 5- دي نيترو بنزوآت و فنول برم دار شده است.
1- ( α – نفتيل اورتان )5/0 گرم از فنول ( کاملاً خشک ) را در يک لوله آزمايش خشک بريزيد و 5/0 ميلي ليتر α – نفتيل ايزوسيانات به آن اضافه نماييد.
چند قطره پيريدين به عنوان کاتاليزور به مخلوط بيافزاييد. اگر واکنش خود به خود صورت نگرفت، مخلوط را براي 10-5 دقيقه روي حمام بخار گرم نماييد. سپس لوله آزمايش را در بشر محتوي يخ قرار دهيد و براي شروع تبلور با بهمزن شيشه يي خراش دهيد. مايع روي رسوب تشکيل شده را جدا نماييد و در صورتيکه لازم است بلورها را روي بوخنر صاف نماييد. براي تخليص محلول را در 16-5 ميلي ليتر ليگروئين داغ (اتر نفت) يا هگزان حل کنيد و براي جدا کردن مواد ناخواسته و دي فنيل اوره که ممکن است موجود باشد محلول را صاف نماييد ( قبلاً قيف را گرم کنيد ). محلول صاف شده را سرد کنيد تا اورتان متبلور شود. سپس بلورها را روي قيف بوخنر صاف نماييد.
2- (3 و 5- دي نيترو بنزوآت)فنولهاي مايع
5/0 گرم 3 و 5- دي نيترو بنزوئيل کلريد را در 5/0 ميلي ليتر فنول حل نماييد و مخلوط را براي 5 دقيقه حرارت دهيد. بگذاريد محلول سرد شود و سپس 3 ميلي ليتر محلول سديم کربنات 5 % و 2 ميلي ليتر آب به آن اضافه نماييد. مخلوط را بشدت بهم بزنيد و چنانچه جامدي در مخلوط موجود است خرد نماييد. محصول را روي بوخنر صاف نماييد و با آب سرد بشوييد. براي تخليص آنرا بوسيله مخلوط حلال اتانول – آب متبلور نماييد.
فنولهاي جامد
5/0 گرم فنول را در 3 ميلي ليتر پيريدين ( خشک ) حل نماييد و 5/0 گرم 3 و 5- دي نيترو بنزوئيل کلريد به آن اضافه کنيد. مخلوط را براي 15 دقيقه رفلاکس نماييد. بگذاريد سرد شود و سپس آنرا به مخلوطي از 5 ميلي ليتر سديم کربنات 5 % و 5 ميلي ليتر آب اضافه کنيد. سپس اين مخلوط را در حمام يخ بگذاريد و بشدت بهم بزنيد تا تمام محصول واکنش بصورت بلورهايي تشکيل شود. رسوبها را با بوخنر صاف کنيد و با آب سرد بشوييد و براي تخليص آنرا با مخلوط حلال اتانول – آب متبلور نماييد.
3- بروموفنول
ابتدا چنانچه محلول برم آماده موجود نيست، بايد آنرا از انحلال 75/0 گرم پتاسيم بروميد در 5 ميلي ليتر آب و سپس 5/0 گرم برم تهيه نماييد. 1/0 گرم فنول را در يک ميلي ليتر متانول يا دي اکسان حل کنيد و سپس يک ميلي ليتر آب اضافه نماييد. حال يک ميلي ليتر مخلوط برم دار کننده را به مايع فنول بيافزاييد و مخلوط را بشدت بچرخانيد سپس افزايش محلول برم دار کننده را قطره قطره و در حاليکه مخلوط را مي چرخانيد ادامه دهيد، محلول برم دار کننده را تا وقتي که رنگ محلول برم باقي بماند بايد اضافه کرده ثابت ماندن رنگ برم در محلول، نشانه پايان واکنش برم دار کردن است. سپس بايد 5-3 ميلي ليتر آب اضافه کرد و مخلوط را بشدت تکان داد رسوبها را روي قيف بوخنر صاف نماييد و با اب بخوبي بشوييد. براي تخليص مشتق تهيه شده آنرا بوسيله مخلوط حلال متانول – آب متبلور نماييد.
در این پست گزارش کار ازمایشگاه شیمی الی را برای شما دوستان قرار دادم تا دوستانی که با روند نوشتن گزارش کار اشنا نیستند و یا مشکلی در نوشتن گزارش کار دارند از این مطالب استفاده کنند.
قصد از ارائه این مطلب ، ارائه گزارش کار اماده نیست. امیدوارم دوستان از این مطلب کمک بگیرند نه کپی برداری !
گزارش کار ازمایشگاه شیمی آلی
دياگرام فازي سيستمهاي سه جزئي
سنتز آسپرین
سنتز استانیلید از آنیلین و استیک انیدرید
سنتز متیل سالیسیلات از سالیسیلیک اسید
کروماتوگرافی کاغذی
فریدل _کرافتس
کلایزن
دانلود کل ازمایش ها در یک فایل
پس از دانلود فایل را از حالت فشرده خارج کنید.
پسورد : www.4800.blogfa.com
کتاب آزمایشگاه شیمی آلی که امروز برای دوستان آماده دانلود شده...
پسورد:(www.y-aspen.loxblog.com
 گزارشکار آزمایشگاه شیمی صنعتی
گزارشکار آزمایشگاه شیمی صنعتی گزارش کار شیمی عمومی2 شناسایی و جداسازی کاتیون های گروه چهارم
گزارش کار شیمی عمومی2 شناسایی و جداسازی کاتیون های گروه چهارم نام آزمایش : تهیه پتاسیم تري اگزالاتو کرومات (III) تري هيدرات
نام آزمایش : تهیه پتاسیم تري اگزالاتو کرومات (III) تري هيدرات آزمایشگاه بیوشیمی1
آزمایشگاه بیوشیمی1 گزارشکار تعیین درصد خلوص مواد شیمیایی
گزارشکار تعیین درصد خلوص مواد شیمیایی دانلود جزوه شیمی عمومی 1
دانلود جزوه شیمی عمومی 1 اتیلن دی آمین تترا استیک اسید (Ethylenediaminetetraacetic acid) (EDTA)
اتیلن دی آمین تترا استیک اسید (Ethylenediaminetetraacetic acid) (EDTA) گزارشکار آزمایشگاه فیزیولوژی جانوری
گزارشکار آزمایشگاه فیزیولوژی جانوری محلول های بافر یا تامپون
محلول های بافر یا تامپون متیل اورانژ چیست و چگونه تشکیل می شود؟
متیل اورانژ چیست و چگونه تشکیل می شود؟ قطره چکان ( Dropper)
قطره چکان ( Dropper) ایمنی در آزمایشگاه
ایمنی در آزمایشگاه آلدئیدها و کتونها (بخش عملى 2): شناسایی و طبقه بندى آلدئیدها و کتونها
آلدئیدها و کتونها (بخش عملى 2): شناسایی و طبقه بندى آلدئیدها و کتونها نرم افزار حرفه ای انجام محاسبات شیمی HyperChem v8.0.7
نرم افزار حرفه ای انجام محاسبات شیمی HyperChem v8.0.7 جدول تناوبی - دارای آرایش الکترونی
جدول تناوبی - دارای آرایش الکترونی احتراق خود به خودی با افزودن آب
احتراق خود به خودی با افزودن آب آتش در کف دست
آتش در کف دست تهيه معرف يونيورسال بوگن
تهيه معرف يونيورسال بوگن عنصر هلیوم
عنصر هلیوم دانلود گزارش کار آزمایشگاه فیزیک 1
دانلود گزارش کار آزمایشگاه فیزیک 1