کمیتی ترمودینامیکی است که میزان خودبهخود انجام شدن یک واکنش را نشان میدهد. این کمیت با G نمایش داده میشود. انجام یک فرآیند از لحاظ ترمودینامیکی هنگامی امکانپذیر است که تغییرات انرژی آزاد گیبس منفی باشد.
انرژی آزاد گیبس را میتوان از این معادلات بدست آورد:
-
این فرمولها دربرگیرندهٔ دو عامل است که در انجامپذیری واکنشها در طبیعت مؤثرند: آنتالپی (انرژی سیستم) و آنتروپی (بینظمی سیستم).
انتالپی (H) تغییرات انرژی ضمن انجام واکنش را دربرمیگیرد. این تغییرات هم انرژی جنبشی راشامل میشود و هم انرژی پتانسیل را، به شرط آن که در حین انجام واکنش فشار وارد بر سیستم ثابت باشد.
یک واکنش زمانی از نظر انرژی انجامپذیر تلقی میشود که بر اثر انجام آن انرژی سیستم کمتر شود. به عبارت بهتر سیستم پایدارتر شود. در این صورت تغییرات انتالپی منفی خواهد بود.
اما در اطراف ما بسیاری از واکنشها اتفاق میافتند که در آنها سیستم گرما میگیرد و انرژی آن افزایش مییابد، یعنی تغییرات انتالپی در آنها مثبت است. این گونه واکنشها به علت عامل دوم رخ میدهند که آنتروپی نامیده میشود و با S نشان داده میشود. این عامل نشاندهندهٔ میزان بینظمی سیستم است و زمانی مساعد است که انجام واکنش سبب زیادشدن بینظمی در سیستم شود. در فرمول انرژی آزاد گیبس عامل S در T ضرب میشود که دمای مطلق (کلوین) گاز است، یعنی اثر عامل بینظمی در دمای بالا بیشتر است.
وجود نقص موجب افزایش در آنتروپی شبکه میشود و بنابراین همه جامدات تمایل به وجود نقص دارند. G = H - TS
افزایشS ، یک جمله منفی در انرژی آزاد وارد میکند. اگر ایجاد نقص گرماگیر باشد،H مثبت میشود ولی ، بزرگتر از صفر خواهد بود و باز هم انرژی آزاد منفیمیشود. با افزایش دما ، نقصها افزایش مییابد و G منفی تر میشود.
قانون اول ترمودینامیک
قانون اول ترمودینامیک به معرفی انرژی درونی ، U ، منجر شد. این کمیت تابع حالتیاست که بر مبنای آن ، مجاز بودن یک فرآیند مورد قضاوت قرار میگیرد وبیان میدارد که فقط تحولاتی مجاز است که انرژی داخلی کل سیستم منزوی ،ثابت بماند. قانونی که ملاک خودبخودی بودن را مشخص میسازد (قانون دوم ترمودینامیک) ، برحسب تابع حالت دیگری بیان میشود. این تابع حالت ،آنتروپی ، S ، است.
ملاحظه خواهیم کرد که بر مبنای آنتروپی قضاوتمیکنیم که آیا یک حالت بطور خودبخودی از حالت دیگری قابل حصول میباشد.در قانون اول با استفاده از انرژی داخلی ، تحولات مجاز مشخص میشود(آنهایی که انرژی ثابت دارند). از قانون دوم با استفاده از آنتروپی ،تحولات خودبخودی از بین همان فرآیندهایی مشخص میشود که بر مبنای قانوناول مجاز میباشد.
بیان قانون دوم
آنتروپی سیستم منزوی در یک فرآیند خودبخودی افزایش مییابد:
که ، آنتروپی تمام قسمتهای سیستم منزوی میباشد.
ازآنجایی که فرآیندهای برگشت ناپذیر (مانند سرد شدن شیئی تا دمای محیط وانبساط آزاد گازها) خودبخودی است، در نتیجه همه آنها با افزایش آنتروپیتوام میباشند. این نکته را میتوان به این صورت مطرح کرد که در فرایندهایبرگشت ناپذیر آنتروپی تولید میشود. از طرف دیگر ، در فرایند برگشت پذیرتوازن وجود دارد، یعنی سیستم با محیط در هر مرحله در تعادل است. هر مرحلهبسیار کوچک در این مسیر برگشت پذیر بوده و پخش نامنظم انرژی روی نمیدهد ودر نتیجه آنتروپی افزایش نمییابد، یعنی در فرآیند برگشت پذیر آنتروپیایجاد نمیشود. آنتروپی در فرآیندهای برگشت پذیر از بخشی از سیستم منزویبه بخش دیگری منتقل میگردد.
تعریف آماری آنتروپی
بر مبنای تعریفآماری ، فرض میشود که در واقع میتوانیم با استفاده از فرمول ارائه شدهتوسط لوودیگ بولتزمن (Ludwing Boltzmann) در سال 1896 ، آنتروپی را محاسبهکنیم:
![[تصویر: KNO3-Solution.jpg]](http://www.chemistmag.com/portal/wp-content/uploads/2011/12/KNO3-Solution.jpg)








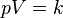
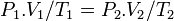
 فشار گاز ایدهآل در قبل از فرآیند
فشار گاز ایدهآل در قبل از فرآیند حجم گاز ایدهآل در قبل از فرآیند
حجم گاز ایدهآل در قبل از فرآیند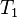 دمای گاز ایدهآل در قبل از فرآیند
دمای گاز ایدهآل در قبل از فرآیند فشار گاز ایدهآل در بعد از فرآیند
فشار گاز ایدهآل در بعد از فرآیند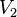 حجم گاز ایدهآل در بعد از فرآیند
حجم گاز ایدهآل در بعد از فرآیند دمای گاز ایدهآل در بعد از فرآیند
دمای گاز ایدهآل در بعد از فرآیند


















