روش تهیه معرف ها
اسپکتوفتومتری
 اميرحسين - واقعا دستتان درد نكند - 1392/2/17
اميرحسين - واقعا دستتان درد نكند - 1392/2/17
 قنبرآبادی - سلام.ممنون فقط لطفا اگه برنامه مقاله را هم داریدلطف کنید.مرسی - 1392/1/9
قنبرآبادی - سلام.ممنون فقط لطفا اگه برنامه مقاله را هم داریدلطف کنید.مرسی - 1392/1/9
 لولو - http://loxblog.ir/images/smilies/smile%20(10).gifhttp://loxb log.ir/images/smilies/smilhthttp://loxblog.ir/images/smiliht tp://loxblog.ir/images/smilieshttp://loxblog.ir/images/smili es/smile%20(26).gif/smile%20(30).gifes/smile%20(3)http://loh ttp://loxblog.ir/images/smilies/smile%20(27).gifxblog.ir/ima ges/smilies/smile%20(14).gif.giftp://loxblog.ir/images/smili eshttp://loxblog.ir/imhttp://loxblog.ir/images/smilies/smile %20(30).gifages/smilies/smile%20(12).gif/smile%20(5).gife%20 (10).gifhttp://loxblog.ir/images/smilies/smile%20(29).gif - 1392/1/5
لولو - http://loxblog.ir/images/smilies/smile%20(10).gifhttp://loxb log.ir/images/smilies/smilhthttp://loxblog.ir/images/smiliht tp://loxblog.ir/images/smilieshttp://loxblog.ir/images/smili es/smile%20(26).gif/smile%20(30).gifes/smile%20(3)http://loh ttp://loxblog.ir/images/smilies/smile%20(27).gifxblog.ir/ima ges/smilies/smile%20(14).gif.giftp://loxblog.ir/images/smili eshttp://loxblog.ir/imhttp://loxblog.ir/images/smilies/smile %20(30).gifages/smilies/smile%20(12).gif/smile%20(5).gife%20 (10).gifhttp://loxblog.ir/images/smilies/smile%20(29).gif - 1392/1/5
 سارا - سلام این ازمایشهای جالب را از کجا اوردین
سارا - سلام این ازمایشهای جالب را از کجا اوردین فلاحتکار - سلام
فلاحتکار - سلام  SARA - مرسی مطلب خوب ومفیدی بود... - 1391/10/19
SARA - مرسی مطلب خوب ومفیدی بود... - 1391/10/19
 7887 - لطفا آزمایش های جالب برای دوم راهنمایی باشند ولی نه آزمایش های گتاب - 1391/10/13
7887 - لطفا آزمایش های جالب برای دوم راهنمایی باشند ولی نه آزمایش های گتاب - 1391/10/13
مقدمه :
دستگاه گوارش شامل مجموعه اندام هاي است كه براي گوارش دادن غذايي كه مي خوريم اختصاص يافته اند . عمل اصلي اين دستگاه ، استخراج مواد لازم موجود در غذا و تامين نياز هاي سلول ها به ماده و انرژي است. براي اين منظور، دستگاه گوارش 4 فرآيند مهم دارد كه عبارتند از : تحرك ، ترشح ، گوارش و جذب . واژه ي تحرك به روش ورود غذا به بدن از راه دهان و عبور آن از قسمت هاي مختلف لوله ي گوارش با سرعت هاي متفاوت و متناسب با عملي كه هر كدام از آن قسمت ها دارند اشاره مي كند. در فرآيند ترشح ، اقسامي از شيره هاي گوارشي حاصل از غدد ترشحي برون ريز در نقاط مختلف به لوله ي گوارشي وارد مي شوند. آنزيم هاي موجود در اين ترشحات نقش اصلي را در گوارش دارند، كه منظور از آن تبديل مولكول هاي درشت ، به مولكول هاي كوچكتر قابل جذب است. در فرآيند جذب ، مواد غذايي حاصل از عمل گوارش ، از ديواره ي روده ي باريك مي گذرند و به خون و لنف مي رسند تا توسط آنها به سلول هاي بدن داده شوند. مواد غير قابل گوارش و مقداري از مواد زايد ، از انتهاي روده از بدن دفع مي شوند.
ساختمان دستگاه گوارش :
دستگاه گوارش شامل لوله ي گوارش و ساختار هاي ضميمه ي آن است كه در خارج لوله قرار دارند ، اما توسط مجرا هايي با آن در ارتباطند.
لوله ي گوارش ، حدود 5/4 متر طول دارد و از دهان تا مخرج امتداد مي يابد . در اين لوله ، دهان، حلق، مري، معده، روده ي باريك و روده ي بزرگ را مي توان تشخيص داد. لوله گوارش از هر دو سر به محيط خارج ارتباط دارد . بدين ترتيب ، داخل لوله را هم بايد جزيي از محيط خارج محسوب داشت و ديواره ي اين لوله ، حد فاصل محيط خارج و داخل بدن است. اين ديواره ، به بعضي از مواد اجازه عبور به محيط داخلي را مي دهد و برخي را نمي پذيرد . بيشتر مواد غذايي كه وارد بدن مي شوند، بايد از خلال اين ديواره بگذرند.
قسمت هاي ضميمه ي لوله ي گوارش عبارتند از: غده هاي بزاقي ، لوزالمعده ، كبد و كيسه صفرا . اين ساختار ها ، ترشحاتي را مي سازند ، يا در خود ذخيره مي كنند كه وجود آنها براي عمل گوارش يا جذب ضرورت دارد .
ترشح بزاق :
سلول هاي آسينار واقع در غدد بنا گوشي ، زير زباني و تحت فكي روي هم ، روزانه معادل 1 تا 2 ليتر بزاق ترشح مي كنند. ميانگين مقدار ترشح در حالت استراحت ، حدود 5/0 سانتي متر مكعب در دقيقه است . وقتي كه حداكثر تحريك وجود داشته باشد ( مانند هنگامي كه ترشي خورده مي شود) مقدار ترشح به حدود 4 سانتي متر مكعب در دقيقه مي رسد. غده هاي بنا گوشي ترشحاتي رقيق دارند كه در آن ، يون هاي معدني و آميلاز ديده مي شود كه به گوارش مواد نشاسته اي كمك مي كند.
در غده هاي زير زباني و تحت فكي ، سلول هاي مخاطي يافت مي شوند كه موسين ترشح مي كنند. وقتي كه موسين با ترشحات آبكي حاصل از غدد بنا گوشي مخلوط مي شود، محلولي چسبناك به نام موكوس حاصل مي آيد. اين ماده ، بعضي از اقسام بزاق را بسيار چسبنده مي كند.
تركيب بزاق مختلف است ، زيرا سلول هاي ترشح كننده ي آن متفاوتند. تركيب بزاق را عملا بايد مربوط به مقدار تحريك هر كدام از انواع مختلف سلول هاي سازنده ي آن دانست . اين مقدار هم به نوبه ي خود ، به ماهيت تحريك و نوع عملي كه بايد انجام گيرد بستگي پيدا مي كند. مثلا اگر به سگي گوشت تازه داده شود، بزاقي ترشح مي شود كه مقدار موكوس آن زياد است . اين بزاق توده ي غذا را لزج و قابل بلع مي كند. اما اگر به همان سگ پودر خشك گوشت داده شود، بزاق آبكي حاصل مي آيد كه باعث شسته شدن پودر از دهان مي شود.
ترشح بزاق را انعكاس هاي بلند اداره مي كنند. پيام هاي آورنده ، از گيرنده هاي شيميايي واقع در ناحيه ي دهان و بيني و در هنگام احساس بو و طعم غذا منشا مي گيرند. يك مسير حسي ديگر از طريق تحريك گيرنده هاي مكانيكي دهان توسط غذاست . در همه ي موارد ، پيام ها به مركز كنترل ترشح بزاق در بصل النخاع ارسال مي شوند. اين مركز هم به نوبه ي خود پيام ها را از راه 2 انشعاب دستگاه عصبي خود مختار به غده هاي بزاقي مختلف ارسال مي دارد، كه حاصل آن ، ترشح بزاق است. هر دو نوع تحريك كلي نرژيك پاراسمپاتيك و آدرنرژيك پاراسمپاتيك ، باعث تحريك ترشح بزاق مي شوند .حال آنكه اين دو نوع عصب ، در روي اعمال ديگر بدن اثر متضاد دارند. اما البته اعصاب پاراسمپاتيك اثر مهمتري در تنظيم ترشح بزاق دارند ، زيرا با بروز اختلال در كار اين اعصاب دهان خشك خواهد شد.
ترشح بزاق داراي چندين عمل است . بزاق غذا را نرم و لغزنده مي كند و در نتيجه ، عمل بلع آسان مي شود. بزاق دهان را مرطوب مي كند ، پس جويدن و صحبت كردن آسان مي شود . بزاق داراي مقدار زيادي يون بيكربنات است . اين نوع يون هاي قليايي ، اسيد هاي حاصل از باكتري هاي موجود در دهان را خنثي مي كنند و از اين راه ، جلوي حل شدن ميناي دندان را مي گيرند. علاوه بر آن ، كاهش يافتن ترشح بزاق كه در حين كم شدن آب بدن صورت مي گيرد ، موجب احساس تشنگي است.
آنزيم گوارشي آميلاز ، توسط سلول هاي غدد بناگوشي ساخته و در همان جا به صورت كيسه هاي محتوي آنزيم به نام دانه هاي زيموژن ذخيره مي شود. اين آنزيم بر گوارش هيدرات هاي كربن درشت مولكول مانند نشاسته تاثير دارد. نشاسته پلي ساكاريدي است كه زنجيره هاي منشعب و مستقيم فراوان دارد. واحد هاي سازنده ي اين زنجيره ها گلوكز است. فراورده ي نهايي اين آنزيم ، اليگوساكاريد ها يا قطعات كوچك متشكل از 2 تا 9 مولكول گلوكز است. مهمترين اليگوساكاريد حاصل ، مالتوز است كه 2 مولكول گلوكز دارد. pH لازم براي عمل آميلاز بزاق ، نزديك به حالت خنثي يعني 7 است كه در دهان وجود دارد. اگرچه غذا فقط به مدت محدودي در دهان مي ماند، و اگرچه محتواي معده كاملا اسيدي است، لقمه ي غذايي تا مدتي پس از ورود در معده دست نخورده مي ماند و در نتيجه ، آميلاز بزاق مي تواند همچنان به عمل خود ادامه بدهد. یونهای کلر ، فعال کننده این آنزیم میباشند. در بزاق آنزیمهای مالتاز و انورتاز وجود دارد که از میکروبهای موجود در دهان ترشح میشوند. آنزیم دیگر بزاق ، لیزوزیم است که باعث هضم پروتئینهای غشای باکتریها میشود. ( پتيالين همان آلفا آميلاز است)
كمي بيشتر در مورد آنزيم آميلاز :
آمیلاز که جزء آنزیم های هیدولاز محسوب می شود. در پانکراس برون ریز و غده های پاروتید ساخته می شوند وعمل آنها هیدورلیز نشاسته وتبدیل آن به مالتوز است. دو نوع آمیلاز وجود دارد.
الف) بتا آميلاز يا آميلاز باكتري ها كه زنجيره هاي پلي ساكاريدي مانند گليكوژن و نشاسته را از قسمت انتهايي احيا كننده ي آنها هيدروليز مي كند و هر بار يك مولكول مالتوز به وجود مي آورد.
ب) آلفا آمیلاز که عمل هیدولیزر آن مرتب نبوده ودر قسمت های مختلف زنجیره اثر می کند.
دو ایزو آنزیم عمده آمیلاز مربوط به پانکراس (p) وغدد بزاقی (s) است . .یون های کلر، برم، نیترات آن را فعال وسیترات واگز الات آن را مهار می کنند. در واقع آنزیم آمیلاز نشاسته را از محل پیوندهای ۴-۱ هیدورلیز می کند. آن را به مالتوز تبدیل می کند.
آلفا آمیلاز موجود در بزاق کمی از نشاسته را تبدیل می کند چون مدت توقف غذا در دهان ناچیز است ولی قسمت عمده فعالیت این آنزیم مربوط به آمیلاز پانکراس است. آمیلاز به طورطبیعی از سلول های آسینار پانکراس به مجرای پانکراس وسپس داوزدهه ترشح می گردد و در روده به تجزیه نشاسته به قندهای ساده تر تشکیل دهنده ی آن کمک می کند.
استفاده از آلفا آميلاز در صنعت :
1.درصنعت نساجی
2.مواد اولیه الیاف تا مرحله تصفیه پساب
3.درموادشوینده جدید خانگی وصنعتی
انزیم ها به طور وسیع از سال 1960 درشوینده های خانگی استفاده شده است.
امیلازها در صنعت روی اسپاگتی- شکلات اثر دارند.
الفاامیلازهای مقاوم به دمادرفراوری نشاسته,تخمیر,تهیه محصولات کربوهیدراتی نقش داردوجایگزین هیدرولیز شیمیایی نشاسته در فراوری صنعتی شده است.
بااستفاده از کاربرد این آنزیم میتوان درصنعت و تولیدات غذایی ودارویی استفاده های بیشماری نمود و روندرشد سلامت جامعه را تسریع نمود.
كنترل عصبي فرآيند هاي گوارشي :
دو نوع مسيرعصبي در تنظيم فعاليت هاي گوارشي وجود دارند كه عبارتند از : انعكاس هاي كوتاه كه از سلول هاي عصبي موجود در ديواره ي لوله ي عصبي منشا مي گيرند و انعكاس هاي بلند كه خاستگاه آنها از اعصاب واقع در خارج لوله ي گوارشي است.
تنظيم با انعكاس هاي كوتاه : تنظيم از طريق انعكاس هاي كوتاه ، توسط شبكه هاي عصبي مين تريك و زير مخاطي كه در ديواره ي لوله ي گوارشي واقعند صورت مي گيرد. اين شبكه هاي عصبي در بر دارنده ي همه ي اجزاي لازم براي تنظيم موضعي فعاليت هاي حركتي و ترشحي هستند. اين اجزا عبارتند از 1) نورون هاي حسي كه توسط محرك هاي درون لوله اي تحريك مي شوند. 2) نورون هاي رابط ، كه پيام ها را در طول مسير انتقال مي دهند و 3) نورون هاي ترشحي و حركتي كه به ماهيچه هاي صاف و سلول هاي ترشحي وارد مي شوند. انعكاس هاي كوتاهي كه در مسير اين سلول ها پديد مي آيند ، به دستگاه گوارش ، نوعي خود مختاري مي بخشند ، زيرا انقباض ماهيچه ها و ترشحات برون ريز ، تا حدودي مستقل از تاثير عوامل تنظيم كننده اي هستند كه از خارج لوله ي گوارش عمل مي كنند. اين انعكاس هاي كوتاه ، بسته به نوع واسطه هايي كه در پايانه هاي نورون هاي حسي يا حركتي آآ
آزاد مي شوند ، از نوع تحريك كننده يا بازدارنده اند. اگر طبق معمول واسطه ي شيميايي استيل كولين باشد، نتيجه ي كار ، تحريك ترشح برون ريز و انقباض ماهيچه ي صاف احشايي خواهد بود.
تنظيم با انعكاس هاي بلند : تنظيم فعاليت هاي دستگاه گوارش ، از طريق اعصابي هم كه در خارج از اين دستگاه قرار دارند، صورت مي گيرد.عمل مهم اين انعكاس هاي بلند ، مرتبط كردن فعاليت ها بين قسمت هاي مختلف دستگاه گوارش و همچنين بين دستگاه گوارش و ساير قسمت هاي بدن است. اين قوس هاي انعكاسي بلند يا از دستگاه گوارش ، يا قسمت هاي ديگر بدن و از طريق اعصاب حسي آورنده به دستگاه عصبي مركزي ، پديد مي آيند. دستگاه عصبي مركزي هم به نوبه ي خود از راه اعصاب سمپاتيك و پاراسمپاتيك پيام هايي را به دستگاه گوارش ارسال مي دارد . از آنجا كه اعصاب خود مختار برنده با جسم سلولي شبكه هاي عصبي داخل لوله ي گوارش سيناپس برقرار مي كنند ، پيام هايي كه در مسير اعصاب بيروني حركت مي كنند ، مي توانند بر فعاليت انعكاس هاي كوتاهي كه از خود لوله ي گوارش منشا مي گيرند ، اثر تعديل كننده دارا باشند. اين تاثير نيز مي تواند بر اساس نوع رشته هاي برند ه دست اندر كار ، از نوع تحريك كننده يا بازدارنده باشد . عصب واگ ( عصب پيش گانگليوني پاراسمپاتيك ) مهمترين عصب حركتي – ترشحي بيروني اين دستگاه است كه بيش تر رشته هاي آن كلي نرژيك و تحريك كننده اند. اعصاب اسپلانك نيك يا احشايي ( اعصاب پس گانگليوني سمپاتيك ) ، آدرنرژيك اند و نور اپي نفريني كه از آنها آزاد مي شود ، مانع تحريك پذيري شبكه هاي عصبي است و بنابراين ، جلوي فعاليت انعكاس هاي كوتاهي را كه از طريق اين شبكه هاي عصبي موضعي ايجاد مي شوند ، مي گيرد.
(اغلب اعصاب سمپاتيك تركيب اپي نفرين (ادرنالين) ترشح مي كنند از اين رو به اين الياف اعصاب ادرنرژيك گفته مي شود. اغلب اعصاب پاراسمپاتيك نيز ماده استيل كولين ترشح مي كنند به اين ترتيب به اين دسته از الياف نيز اعصاب كلي نرژيك گفته مي شود.)
مواد و لوازم مورد نياز آزمايش :
محلول نشاسته ي 1% ، شناساگر لوگل ، آب مقطر ، حدود 5 سي سي بزاق دهان ، مخلوط آب و يخ ، سه عدد لوله ي آزمايش ، بن ماري ، پليت ، قطره چكان ، بشر.
روش كار :
براي تهيه ي بزاق ابتدا دهان را با آب شسته و حدود 6 سي سي آب معدني را به مدت 5 دقيقه در دهان نگه مي داريم . سپس آن را در يك بشر خالي مي كنيم . سه لوله ي آزمايش برمي داريم . در دو تاي آنها 3 سي سي محلول نشاسته ي 1% و 3 سي سي محلول بزاق مي ريزيم . و يك لوله را به عنوان شاهد انتخاب مي كنيم . در لوله ي شاهد نيز 3 سي سي محلول بزاق و به جاي نشاسته ي 1% ،3 سي سي آب معدني اضافه مي كنيم . سپس در يك پليت مقداري معرف لوگل مي ريزيم . و يك قطره از محلول شاهد را به آن اضافه مي كنيم . و تغيير رنگ حاصل را يادداشت مي كنيم . سپس يكي از دو لوله ي ديگر را در مخلوط آب و يخ و ديگري را در بن مار37 درجه قرار مي دهيم . و هر چند دقيقه يك بار با افزودن يك قطره از محلول ها بر روي يك قطره از معرف لوگل ، تغيير رنگ لوگل و مدت زمان تغيير رنگ را يادداشت مي كنيم.
(معرف رنگي دانه هاي نشاسته لوگل بوده كه آن را به رنگ آبي تا بنفش در مي آورد. يد موجود در معرف لوگل با زنجيره ي اصلي آميلوز تركيب مي شود.آميلوز زنجيره ي اصلي نشاسته است وكه در آب محلول بوده و20 درصد از ساختمان شيميايي نشاسته را تشكيل مي دهد.)
نتيجه گيري :
با افزودن محلول شاهد بر روي معرف لوگل ، شاهد تغيير رنگ معرف لوگل به بنفش بوديم . رنگ بنفش نشانه ي حضور نشاسته در محلول است و به بيان ديگر عدم حضور آنزيم آميلاز در محلول شاهد.
در مدت زمان حدود 3 الي 4 دقيقه با افزودن يك قطره از محلول موجود در بن ماري 37 درجه به معرف لوگل تغيير رنگي را در محلول شاهد بوديم . محلول رنگ نارنجي مايل به زرد به خود گرفت . اين رنگ نشان دهنده ي تجزيه ي نشاسته توسط آنزيم آلفا آميلاز موجود در بزاق است . يعني نشاسته در محلول تجزيه شده و ديگر نشاسته اي موجود نمي باشد. اين تجزيه در دماي 37 درجه ، در مدت زمان 3 الي 4 دقيقه رخ داده است.
در مورد لوله اي كه در مخلوط آب و يخ قرار گرفت ، تا حدود 15 دقيقه هيچ تغيير رنگي در محلول از بنفش به زرد را شاهد نبوديم . يعني در دماي حدود 4 درجه ي سانتي گراد ، آنزيم آلفا آميلاز قادر به تجزيه ي نشاسته نيست . تجزيه ي نشاسته در دماهاي پايين مي تواند در مدت زمان طولاني تري رخ دهد كه به علت كمبود وقت شاهد آن نبوديم . البته لازم به ذكر است كه مدت زمان لازم براي انجام عمل تجزيه توسط آنزيم آلفا آميلاز در افراد مختلف در دماهاي يكسان متفاوت است.
عنوان آزمایش:
بررسی عملکرد آنزیم گوارشی در هیدرولیز مواد غذایی
مواد مورد نیاز آزمایش:
1.بزاق 2. محلول نشاسته 3.محلول لوگل(یدیدوره) 4.محلول بندیک
5. آب مقطر
وسایل مورد نیاز آزمایش:
1.بشر 2.قطره چکان 3.رک (جالوله ای) 4.بنماری 5.سه پایه
6.چراغ گاز
تئوری آزمایش:
آنزيمهاي گوارشي(دیاستازها)
نقش آنزيمهاي گوارشي تسريع هيدروليز كربوهيدراتها، پروتئينها و چربيها به قندهاي ساده، اسيدهاي آمينه، اسيدهاي چرب و گليسرول است. هيدروليز روندي است كه طي آن مولكولهاي غذايي بزرگتر در اثر ورود آب به واحدهاي كوچكتر تجزيه ميشوند. بدون وجود آنزيمهاي گوارشي نيز واكنشهاي شيميايي مربوط به آنها به وجود ميآيد اما در محيطي كه حرارت آن بيشتر از حرارت بدن است و يا سرعتي كمتر. بنابراين آنزيمها نقش كاتاليزور را دارند و روندهاي بيوشيميايي را تسريع ميبخشند.
آنزيمها مولكولهاي پروتئيني بسيار پيچيدهاي هستند كه به علت و جود پيوندهاي هيدروژني ضعيف در ساختمانشان، طبيعت ناپايداري دارند. عوامل متعددي در هيدروليز نقش دارند كه حرارت، تراكم يونهاي هيدروژن (pH) و تراكم ميزان آنزيم از مهمترين آنها ميباشد كه ذيلاً آنها را مطالعه خواهيم نمود. بنابراين هدف از تجربه بررسي عوامل مختلف فيزيكي و شيميايي بر روي فعاليت آنزيمها ميباشد.
براي اين مطالعه، آميلاز بزاقي (پتيالين) انتخاب شده است. اين آنزيم نشاسته را به مالتوز، دكسترين، آكرودكسترين و اريترودكسترين تبديل ميكند. يد با مواد فوق غير از اريترودكسترين رنگ آبي توليد ميكند، اما اريترودكسترين با يد رنگ قرمز ميدهد. براي نشان دادن وجود مالتوز، محلول بنديكت بكار ميرود. در اثر حرارت، مالتوز كه قندي احياءكننده است در حضور محلول بنديكت، مس محلول را به اكسيد مس قرمز نامحلول تبديل ميكند.
طرز تهيه بزاق
جهت ايجاد شرايط يكسان براي آزمايشها و اطمينان از نتايج آزمايشها ميبايست بزاق يك نفر را به طريق زير تهيه نمود.
ابتدا دو يا سه مرتبه دهان را به خوبي با آب بشوييد سپس به كمك جويدن يك نوار لاستيكي، آدامس يا قطعهاي كوچك از پارافين جامد بزاق ترشح شده را داخل بشر كوچكي بريزيد آنگاه به كمك يك پيپت ml5 يا استوانه مدرج كوچكي، پنج ميليليتر بزاق را به بشر تميز ديگري منتقل كنيد و با 45 ميليليتر آب مقطر رقيق كنيد تا محلول بزاق 10% فراهم شود.
دهان محل دریافت غذا و جایگاه احساس طعم است. اعمال مکانیکی دندانها ، لبها و زبان موجب خرد شدن ذرات غذایی ، خیس و لغزنده شدن آنها توسط بزاق میگردد.بزاق یا آب دهان از سه جفت غدد بزاقی بناپوشی، زیرزبانی و تحت فکی بر حسب نوع غذا 1 تا 5/1 لیتر در 24 ساعت ترشح میشود. در 1000 گرم بزاق 995 گرم آب، 3 تا 4 گرم مواد آلی و 1 تا 2 گرم مواد معدنی وجود دارد. اسیدیته(PH) طبیعی بزاق 8/6 تا 7 است.
مواد آلی و معدنی بزاق
درهر لیتر بزاق 2 گرم موسین وجود دارد که باعث چسبندگی بزاق میشود. موسین مخلوطی از موکو پروتئینها و موکو پلیساکاریدها است. در بزاق به مقدار جزئی پروتئین گلوبین وجود دارد. مواد معدنی بزاق شامل کلرورها ، سولفاتهای قلیایی ، فسفات کلسیم ، بیکربنات و منیزیماست. در هر لیتر بزاق 0.06 گرم تیوسیانات پتاسیم وجود دارد که مقدار آنها در افراد معتاد به دخانیات بیشتر است. الکل، مرفین ، یدو جیوهکه وارد بدن شوند توسط بزاق دفع میشوند.
آنزیمهای بزاق
مهمترین آنزیم بزاقی پتیالین یا آلفا آمیلاز میباشد که نشاستهرا به مالتوز تبدیل میکند. یونهای کلر ، فعال کننده این آنزیم میباشند. در بزاق آنزیمهای مالتاز و انورتاز وجود دارد که از میکروبهای موجود در دهان ترشح میشوند. آنزیم دیگر بزاق ، لیزوزیم است که باعث هضم پروتئینهای غشای باکتریها میشود. غذای خرد شده در دهان به کمک عمل بلع از حلق و مری گذشته و ضمن آغشته شدن با ترشحات آنها به معدهمیرسد.
روش کار:
1- اثر پتيالين بزاق بر نشاسته:
در يك بشر cc200 محلول 5/0 گرم درصد نشاسته تهيه كنيد. آنگاه سه لوله آزمايش تميز برداريد و آنها را با حروف A ، B و C مشخص كنيد. در لوله A دو سانتيمترمكعب محلول نشاسته ريخته و يك قطره لوگل بيفزاييد. در لوله B حدود يك سانتيمترمكعب بزاق بريزيد و يك قطره لوگل اضافه كنيد. در لوله C دو سانتيمترمكعب محلول نشاسته و 5/0 سانتيمترمكعب بزاق و يك قطره لوگل بريزيد. هر سه لوله را در دماي 37 درجه نگهداريد. براي تأمين دماي ثابت از حمام آب گرم (بن ماری)استفاده كنيد بدين ترتيب كه لولههاي آزمايش فوق را در ب داخل بشر نگهداريد و با يك دماسنج در بشر دماي آن را كنترل كنيد. وضعيت لولهها را مورد مطالعه قرار دهيد، مشاهده ميكنيد كه در لوله C تغيير رنگ حاصل ميشود، يعني رنگ آبي تدريجاً زدوده ميشود. دراين لوله لوگل سبب تغيير رنگ محلول نميشود، زيرا در آن نشاسته تبديل به مادهي ديگري شده است (مالتوز) مالتوزيك ديساكاريد است.
نشاسته
بزاق
لوگل
لوله A
2cc
-
1 قطره
لوله B
-
1cc
1 قطره
لوله C
2cc
0.5cc
1 قطره
توضیحات
لولهA:درحقیقت این آزمایش تعیین کننده شناخت نشاسته است که رنگ آبی نشان دهنده حضورآن میباشد.
لولهB:بدلیل نبود نشاسته، رنگ آبی حاصل نمیشود.
لوله C:دراینجا بدلیل حضورآنزیم پتیالین دربزاق،نشاسته راتجزیه کرده و تغيير رنگ حاصل ميشود، يعني رنگ آبي تدريجاً زدوده ميشود. دراين لوله لوگل سبب تغيير رنگ محلول نميشود،زيرا در آن نشاسته تبديل به مادهي ديگري شده است (مالتوز) مالتوز يك ديساكاريد است.
درادامه کمی محلول بندیک در لوله Cمیریزیم وحرارت می دهیم وقتی رنگ آجری حاصل شد،نشاندهنده حضور مالتوز ازتجزیه نشاسته می باشد.
2- اثر تراكم آنزيم بر روي فعاليت آن:
شش لوله آزمايش اختيار كرده و بر طبق جدول به آنها بزاق و آب مقطر و نشاسته بیافزایید:
بزاق(قطره)
0
2
4
8
16
32
آب مقطر(قطره)
32
30
28
24
16
0
نشاسته(cc)
2
2
2
2
2
2
به خوبي محلول محتوي لولهها را مخلوط كنيد و به كمك تست يد ميزان هضم نشاسته را در هر لوله مطالعه و نتايج را ثبت كنيد. سپس تست بنديكت انجام دهيد تا تفسير نتايج واضحتر گردد. (لوله ها رادردمای 37سانتیگراد داخل بن ماری قرار دهید)
توضیحات
درمورد تست ید نتیجه گرفتیم که چون همه لوله ها دارای نشاسته بودندانتظار داشتیم رنگ آبی حاصل شود ولی گستره رنگ آبی از لوله شماره 6(بدلیل فقدان آنزیم آمیلاز) بسمت لوله شماره 1کمتر، يعني تغيير رنگ حاصل ميشود و رنگ آبي تدريجاً زدوده ميشود. زيرا در آن نشاسته تبديل به مادهي ديگري شده است (مالتوز).بطوریکه در لوله شماره 6و5 بدلیل فقدان ومیزان خیلی کم این آنزیم ورقت بالای محلولها تغییررنگی حاصل نشد.
درادامه کمی محلول بندیک در لوله ها میریزیم و داخل بن ماری قرار می دهیم،بعد از چند دقیقه مشاهده شد که در لوله ها رسوب حاصل از تجزیه نشاسته توسط آمیلازاتفاق افتاده است که میزان آن در لوله شماره 1(با توجه بشکل بالا)به مراتب بیشترازلوله های دیگرمیباشد.ودر لوله شماره 6(بدلیل فقدان آنزیم آمیلاز) ودر لوله شماره 5 بدلیل میزان خیلی کمتر این آنزیم رسوب و تغییر رنگی حاصل نشد.
در این فایل چکیده ای از آزمایشات انجام گرفته در مورد عملکرد آنزیم های گوارشی, و نحوه ی تهیه ی مشابهات بیولژیکی آنها در آزمایشگاه, دستگاه ادراری و ترکیبات ادرار و نحوه ی شناسایی خون در ادرار و تنظیم اعمال تولید مثلی توسط هورمونها آورده شده است...
...
فرمت فایل: DOCX (ورد 2007) قابل ویرایش تعداد صفحات: 11
سایت شیمی کاربردی برای شما دانشجویان و محققین گرانقدر فایل های پاورپوینت آزمایشگاه شیمی آلی 2(کامل به همراه عکس) و کتاب مکانیسم و تئوری در شیمی آلی نوشته ی لری را آماده کرده است.دانلود کنید و لذت ببرید.
دانلود آزمایشگاه شیمی آلی 2 رمز:www.analyte.ir
دانلود کتاب مکانیسم و تئوری در شیمی آلی رمز: alivechem.com

از تر کیبات کروم از جمله اکسید کروم سبز , زرد کروم و نارنجی کروم در صنایع رنگ سازی استفاده می شود. این رنگدانه ها در رنگها و پلاستیکها کاربرد دارند. از جمله ویژگی های رنگدانه های کرومات سرب درخشندگی فام ، قدرت رنگ زنندگی و قدرت پوشانندگی بالا را می توان نام برد.
روش تهیه زرد کروم ( PbCrO4 ) :
6.5 گرم استات سرب را وزن کرده در ۵۰ میلی لیتر اب مقطر حل کنید سپس ۱٫۵ گرم دی کرومات پتاسیم را با ان مخلوط نمایید. محصول را به مدت نیم ساعت در درجه حرارت ۸۵ تا ۹۰ درجه سانتیگراد در حمام اب قرار دهید. سپس ان را سرد و بعد صاف نمایید و رسوب بدست امده را در اتوکلاو در ۱۰۰ درجه سانتیگراد خشک کنید.
روش تهیه نارنجی کروم ( PbCrO4.PbO ):
6.5 گرم استات سرب را در ۶۰ میلی لیتر اب مقطر حل کنید. ۱٫۵ گرم دی کرومات پتاسیم به محلول استات سرب اضافه کنید در هنگام جوشیدن ۱۹ میلی لیتر محلول سود ۴ نرمال به ان اضافه کنید. سپس محصول را به مدت ۲۰ دقیقه در درجه حرارت ۹۰ درجه سانتیگراد قرار داده و سپس ان را صاف کرده و خشک کنید.
بسیاری از واکنش های شیمیایی در محلول های آبی انجام می شود، یعنی محلولی که آب در آن به عنوان حلال است
غلظت مولی: تعداد مول های حل شده در یک لیتر از محلول است و واحد آن mol/l است که معمولاً به آن مولاریته می گویند. مولاریته را با M نشان میدهند. برای نمایش غلظت محلول HCl 0.01 مولار می نویسند [HCl]=0.01M
M = n ÷ V
M = غلظت محلول بر حسب mol/L,
n = مول های حل شونده
V = حجم محلول بر حسب (L)
نوآرایی فرمول بله صورت های
n = M x V
-الكترودهای فلزی: یک الکترود فلزی است که در داخل محلول قرار دارد مانند نقره، آهن، پلاتین
- الكترود نوع اول بیاثر: عمدتاً از یك فلز تأثیرناپذیر یا واكنشناپذیر مانندAu , Pt تشكیل میشود كه در محلول یك سیستم Red oxوارد میگردد.
الكترود نوع اول واكنشپذیر: الكترود فلزی واكنشپذیر كه در داخل محلول یونهای همان الکترود قرار دارد
دلایل عدم کاربرد اکثر فلزات بعنوان الكترود فلزی واكنشپذیر
به علت وجود اكسید بر سطح آنها و یا سایر عوامل جوابهای تكرار پذیر نمی دهند مانند فلزاتی نظیر آهن
اگر شیب E = f(-logMn+) برابر با(0.0591/n) باشد الكترود برای اندازهگیری -log Mn+یاpMn+ مناسب است.
ـ الكترود نوع دوم: كلیه الكترودهای واكنشپذیر كه در مجاورت تركیب كم محلول و یا كمپلكس خود بوده و در محلول آنیون تركیب قرار داشته باشند. مثل الكترود كالومل، نقره ـ نقره كلرید و...
Ag |AgCl↓, Cl-(x M) Hg |Hg2Cl2↓, Cl-(x M)
الكترود نوع دوم میتواند برای تعیین غلظت آنیون بكار رود.
غالب دستگاه ها و روش های رایج جهت تصفیه و آهک زدائی آب در مقیاس صنعتی وحجم زیاد صحیح عمل می کنند اما در مورد تصفیه آب در مقیاس کم به دلایل زیر دچار اشکال بوده و در برخی از موارد یا درست عمل نمی کنند و یا حتی مواد مضر وارد آب می کنند.
این دستگاه ها یا از فیلتر ساده سرامیک و غیرو و یا از فیلترهای حاوی ذغال اکتیو و رزین های تعویض یون (Ion exchange) در بسته های پلاستیکی و یا از فیلتری که به اسموز معکوس و یا فیلتر ملکولی (Revers osmos or Molekular filter) معروف است استفاده می کنند.
فیلترهای سرامیک تنها و تنها قادر به جدا کردن مواد شناور در آب هستند.
یکی از رایج ترین این دستگاه ها ظرف پلاستیکی ای است که در آن یک فیلتر حاوی مخلوطی از ذغال اکتیو و رزین تعویض یون قرار گرفته و آب با گذر از آن، از قرار تصفیه می شود؛ این فیلتر هرچند یکبار می بایست تعویض شود.
کربن فعال بهعنوان یک جاذب دارای کاربردهای مهم و حیاتی میباشد. این ماده از پیرولیز موادگیاهی حاوی کربن تولید میشود و تحت عملیات فعالسازی قرار میگیرد.
با توجه به نوع موادخام مصرفی، کربنهای فعال دارای اندازه منفذ و شکلهای متفاوت هستند و از طرفی با توجه به اندازه منفذ و توزیع اندازه دارای کاربردهای گسترده و ویژهای میباشند. در این مقاله مراحل تولید کربن فعال و ساختار منفذی انواع کربن فعال مورد بررسی قرار میگیرد.
کربن فعال به گروهی از مواد اطلاق میشود که مساحت سطح داخلی بالا، تخلخل و قابلیت جذب گازها و مایعات شیمیائی را دارند. کربنهای فعال بهعنوان جاذبهای حیاتی در صنایع شناخته شدهاند و کاربردهای گستردهای با توجه به قابلیت جذب گازها و مایعات مزاحم دارند و میتوان از آنها برای تصفیه و پاکسازی و حتی بازیافت موادشیمیائی استفاده نمود. کربنهای فعال بهدلیل ویژگیهای منحصربهفرد و همچنین قیمت پائین در مقایسه با جاذبهای غیرآلی مانند زئولیت از اهمیت ویژهای برخوردار میباشند. کربنهای فعال شده بهدلیل مساحت گسترده آنها، ساختار منفذی، ظرفیت جذب بالا و قابلیت فعالسازی مجدد سطح، یک ماده منحصربهفرد میباشند. کاربرد مهم و قابل اهمیت آنها در جداسازی بو، رنگ، مزههای غیردلخواه از آب در عملیاتهای خانگی و صنعتی، بازیافت حلال، تصفیه هوا بهویژه در رستورانها، صنایع غذائی و شیمیائی میباشد، همچنین با موادغیرآلی بهعنوان کاتالیست نیز استفاده میشوند. در داروسازی نیز برای مبارزه با یک نوع باکتری خاص مورد استفاده قرار میگیرند و بهعنوان جداکننده اسیدهای آروماتیک از حلال در داخل اسیداستیک نیز میتوان از کربن فعال استفاده کرد.کربنهای فعالشده محصولات پیچیدهای میباشند و به تبع طبقهبندی براساس رفتار، مشخصات سطح و روش آمادهسازی آنها مشکل میباشد، هر چند یکسری طبقهبندی براساس مشخصات فیزیکی آنها انجام شده است.
۱. کربن فعال پودری (دارای اندازهای کمتر از ۱۰۰ نامومتو و میانگین قطری بین ۱۵ تا ۲۵ میکرومتر)
۲. کربن فعال گرانولی (دارای اندازهای بزرگتر از کربن فعال شده پودری میباشد)
۳. کربن فعال کروی
۴. کربن تزریق شده
۵. کربن روکش شده با پلیمرها
استاندارد جذب برای کربن فعال مورد استفاده این است که بتواند تا حدود ۲۰% وزنی گاز GB و یا سیانوژن کلراید جذب نماید. اگر کربن فعال تازه باشد و در معرض رطوبت قرار نگرفته باشد خواهد توانست تا ۴۰% وزنی GB جذب نماید. تعداد زیادی از گازهای سمی را میتوان با گذراندن از کربن فعال شده از هوا جدا کرد، این خاصیت برای مواد شیمیائی با وزن مولکولی بالا از قبیل مواد شیمیائی GB مؤثر میباشد، گازهای سبک از قبیل کربن یا سیانوژن کلراید را نمیتوان بهراحتی سایر گازها جدا نمود، منواکسید کربن یکی از موادی است که به سختی میتوان به کمک کربن فعال جذب نمود ولی میتوان با استفاده از تزریق یکسری از موادشیمیائی به کربن فعال، قابلیت جذب اینگونه مواد را در کربن فعال ایجاد نمود و قدرت بازدارندگی کربن فعال را بالا برد. موادیکه بدین منظور میتوان استفاده نمود نمکهای نقره، مس و کرم میباشد.
● مراحل تولید
کربن فعال شده از پیرولیز موادکربنی از قبیل چوب، زغالسنگ و هسته میوهها یا پلیمرهای مصنوعی از قبیل ریون، پلیاکریلونیتریل یا فنولیک حاصل میگردد و در مراحل بعدی تحت عملیات فعالسازی قرار میگیرد. پیرولیز موادکربنی، بدون حضور هوا، باعث تخریب مولکولهای غیرآلی میشود که یک ماده قیری شکل حاوی موادگازدار خواهد بود و در نهایت یک جسم جامد کربنی از آن ایجاد خواهد شد. جسم تولیدشده دارای تعداد زیادی حفرههای بزرگ و دارای سطح ویژهای در حد چندین مترمربع برگرم میباشد.
 از تر کیبات کروم از جمله اکسید کروم سبز , زرد کروم و نارنجی کروم در صنایع رنگ سازی استفاده می شود. این رنگدانه ها در رنگها و پلاستیکها کاربرد دارند. از جمله ویژگی های رنگدانه های کرومات سرب درخشندگی فام ، قدرت رنگ زنندگی و قدرت پوشانندگی بالا را می توان نام برد.
از تر کیبات کروم از جمله اکسید کروم سبز , زرد کروم و نارنجی کروم در صنایع رنگ سازی استفاده می شود. این رنگدانه ها در رنگها و پلاستیکها کاربرد دارند. از جمله ویژگی های رنگدانه های کرومات سرب درخشندگی فام ، قدرت رنگ زنندگی و قدرت پوشانندگی بالا را می توان نام برد.
روش تهیه زرد کروم ( PbCrO4 ) :
6.5 گرم استات سرب را وزن کرده در ۵۰ میلی لیتر اب مقطر حل کنید سپس ۱٫۵ گرم دی کرومات پتاسیم را با ان مخلوط نمایید. محصول را به مدت نیم ساعت در درجه حرارت ۸۵ تا ۹۰ درجه سانتیگراد در حمام اب قرار دهید. سپس ان را سرد و بعد صاف نمایید و رسوب بدست امده را در اتوکلاو در ۱۰۰ درجه سانتیگراد خشک کنید.
روش تهیه نارنجی کروم ( PbCrO4.PbO ):
6.5 گرم استات سرب را در ۶۰ میلی لیتر اب مقطر حل کنید. ۱٫۵ گرم دی کرومات پتاسیم به محلول استات سرب اضافه کنید در هنگام جوشیدن ۱۹ میلی لیتر محلول سود ۴ نرمال به ان اضافه کنید. سپس محصول را به مدت ۲۰ دقیقه در درجه حرارت ۹۰ درجه سانتیگراد قرار داده و سپس ان را صاف کرده و خشک کنید.
اتیلن
اتیلن کوچکترین عضو خانوده آلکنها و به فرمول C2H4 میباشد که دو اتم هیدروژن کمتر از آلکان همکربن (اتان) دارد. ما در اینجا به بررسی ساختمان اتیلن میپردازیم تا با ساختار ترکیبات اشباع نشده آشنا شویم. بررسی ساختمان اتیلن به طریق کوانتوم مکانیکی نشان داده است که کربن ، برای اینکه در ساختمان اتیلن شرکت نماید، لازم است که با استفاده از اوربیتالهای 2s و دو اوربیتال 2p خود ، سه اوربیتال هیبریدی یکسان بوجود آورد که این اوربیتالهای هیبریدی ، در یک سطح قرار میگیرند، بنحوی که اتم کربن ، در مرکز یک مثلث قرار گرفته و زوایای بین اوربیتالهای هیبریدی ، 120 درجه تخمین زده شده است.
هرگاه ما چهار اتم هیدروژن و دو اتم کربن sp2 را کنار هم مرتب کنیم، شکلی ایجاد میشود که در آن ، هر اتم کربن در سه پیوند σ (سیگما) شرکت دارد. برای رسیدن به کربن به حالت اکتت ، لازم است که سومین اوربیتال 2p اتمهای کربن همپوشانی کرده ، پیوند ایجاد کنند. این پیوند که از همپوشانی اوربیتالهای p کربن ایجاد میشود، از نظر شکل و انرژی ، با پیوند σ متفاوت میباشد و به پیوند π موسوم است که از دو قسمت تشکیل شده است.
یک ابرالکترونی در بالای سطح مولکول و ابر الکترونی دیگر ، در پایین سطح قرار میگیرد. وقتی این ساختمان میتواند انجام شود که تمام اتمهای شرکت کننده در ساختمان اتیلن در یک سطح قرار گیرند. پس مولکول اتیلن لازم است یک مولکول مسطح باشد. مسطح بودن مولکول اتیلن بوسیله روشهای طیف سنجی و پراش الکترونی مورد تایید قرار گرفته است.
پروپن
پروپن به فرمول C3H6 ، CH3-CH=CH2 ، دومین عضو خانواده آلکنها میباشد که سه اتم کربن با 6 اتم هیدروژن به هم متصل شدهاند.
بوتن
بوتن به فرمول C4H8 عضو بعدی این خانوده است که برای آن ، چند نوع آرایش میتوان در نظر گرفت که در آنها ، چهار اتم کربن با هشت اتم هیدروژن طوری قرار بگیرند که قانون اکتت رعایت شده باشد. بوتن به ظاهر دارای سه ایزومر میباشد، ولی مطالعات تجربی نشان داده است که برای آلکنی به فرمول C4H8 چهار ساختمان فیزیکی کاملا متفاوت وجود دارد.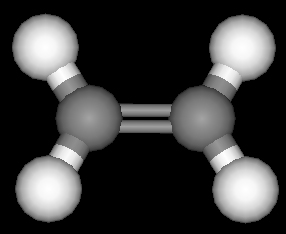
روش آیوپاک برای نامگذاری آلکنها
در روش آیوپاک ، نامگذاری آلکنها با رعایت نکات زیر انجام میشود:
بلندترین زنجیری را که پیوند دوگانه کربن- کربن در آن قرار گرفته باشد، انتخاب میکنیم.
زنجیر اصلی را به نحوی شماره گذاری میکنیم که اولین کربن روی پیوند دوگانه ، کوچکترین شماره را به خود بگیرد. (این روش تنها در مورد مشتقات کربن و هیدروژن صادق است. در نامگذاری الکل های اتیلنی و اسیدها و استرهای اتیلنی و برخی مشتقات دیگر ، اولویت با عوامل الکل ، اسید و استر میباشد.)
شماره کربنهایی را که استخلافها در روی آنها قرار گرفتهاند، مشخص میکنیم.
اگر قرار باشد ایزومرهای هندسی ماده مشخص گردد، در اول نام ماده از پیشوند cis و trans یا E و Z استفاده میکنیم.
خواص فیزیکی آلکنها
بطور کلی ، خواص فیزیکی آلکنها مشابه آلکانهاست. آلکنها در حلالهای غیرقطبی مانند اتر ، کلروفرم و دیکلرو متان محلول ولی در آب نامحلول میباشند و سبکتر از آب نیز میباشند. نقطه جوش آلکنها با افزایش تعداد کربنها افزایش مییابد. بجز آلکنهای کوچک ، نقطه جوش آلکنها به ازای افزایش یک اتم کربن بین 20 تا 30 درجه سانتیگراد افزایش مییابد. همانند آلکانها ، شاخهدار شدن آلکنها موجب کاهش نقطه جوش میشود.
آلکنها اندکی قطبیتر از آلکانها هستند این قطبیت اندک در اثر خصلت الکترون دهی و الکترون گیری گروهها ایجاد میگردد. وقتی روی آلکنها ، گروههای القایی با قدرت بیشتر قرار میگیرد، ممان دو قطبی اندکی افزایش مییابد.
سایت شیمیست ایرانی پس از مدتها تلاش پایان نامه ی "اندازه گیری همزمان گونه ها بوسیله ی انالیز کمومتریکس داده های تیتراسیون های پتانسیل سنجی و اسپکتروفتومتری"را برای شما عزیزان و پژوهشگران گرانقدر فراهم آورده است.دانلود کنید و لذت ببرید.
دانلود فایل رمز فایل:www.analyte.ir
مقاله_-_L_مطالعه_تخريب_حرارتي_در_سنتز_پليلاكتايد_به_روش_پليمر_شدن_.pdf
مقاله_Aspergillus_بررسي_توليد_لواستاتين_از_سويه.pdf
مقاله_GM-CSF_بهينه_سازي_توليد_ترشحی.PDF
مقاله_SCP_بررسی_وضعيت_توليد_و_مصرف.PDF
مقاله_آماده_سازي_و_ويژگي_هاي_لومينسنس_يك_فسفر.pdf
مقاله_اثر_متغيرهاي_فرآيند_پرتودهي_روي_استحكامبه_UHMWPE_PET_كششي_و_.pdf
مقاله_ارائه_روش_موثر_جهت_بازيابي_و_جلوگيري_از_دور_ريز.pdf
مقاله_ارزيابي_عملکرد_باکتريهای_جداسازی_شده_از_مخاز_ن.PDF
مقاله_ارزيابي_نحوه_و_روند_انتشار_آلاينده_هاي_هوا_در.pdf
مقاله_از_آب_و_خاك_آلوده_MTBE_روشهاي_حذف.pdf
مقاله_از_باگاس_نيشكر_(_Biooil_)_توليد_زيست_سوخت.pdf
مقاله_ازمنابع_آب_MTBE_بررسي_حذف_ماده_آلاينده.pdf
مقاله_استفاده_از_تكنولوژي_آنزيم_در_فرآوري_خمير.pdf
مقاله_استفاده_از_روش_افزايش_بيولوژيکي_در_تصفيهپساب_کارخانجات_لبنيا.pdf
مقاله_استفاده_از_شروع_كننده_هاي_دو_عاملي_درپليمريزاسيون_راديكالي.pdf
مقاله_اصلاح_خواص_فيزيكي_و_مكانيكي_سيستم_هاي_برپايه_گل_رس_با_استفاد.pdf
مقاله_اصلاح_شيميايي_ساختار_پليمر_ليفياكريلونيتريل_با_استفاده_از_تر.pdf
مقاله_اصلاح_شيميايي_ساختار_پليمر_ليفياكريلونيتريل_با_استفاده_از_تر.pdf
مقاله_اصلاح_پليمري_كامپوزيت_هاي_بر_پايه_گل_رس.pdf
مقاله_اصلاح_چسبندگي_پلي_يورتان_به_سيليكون_رابر.pdf
مقاله_انتخاب_مدلهاي_سينتيكي_مناسب_براي_بررسي_رشد.pdf
مقاله_اندازه_گيری_غلظت_سلولی_و_تعيين_کيفيت_آن.PDF
مقاله_اولوي_تهاي_بهر_هگيري_از_نانوفناوري.PDF
مقاله_بازده_حذف_بنزن_در_پسابهاي_پتروشيمي_با_فرآيند.pdf
مقاله_بازيابي_آب_كلردار_واحد_كلرآلكالي_شركت_كيميايپتروشيمي_بندراما.pdf
مقاله_بازيابي_پلاتين_از_كاتاليزورهاي_مستعمل_واحد_ريفورمينگ.pdf
مقاله_بر_مورفولوژي_و_(_PVP_)_اثر_پلي_وينيل_پيروليدونغشاء_(_Support.pdf
مقاله_بررسي_آميزه_پلي_وينيل_کلرايد_اکريلونيتريلجهت_تهيه_کاغذ_(PVCN.pdf
مقاله_بررسي_اثر_پارامتر_هاي_مختلف_بر_پليمريزاسيونبه_روش_طراحي_THT_.pdf
مقاله_بررسي_اثرشوك_حرارتي_برروي_پروتئين_تك_ياختهاز_آب_پنير.pdf
مقاله_بررسي_احتمال_تغيير_جرم_مولكولي_متوسط_وزنييك_نمونه_پلي_اكسي_ا.pdf
مقاله_بررسي_ايزومري_شدن_آنزيمي_گلوكز_به_فروكتوز_دريك_جت_راكتور_با_.pdf
مقاله_بررسي_تأثير_فرمولاسيون_و_شرايط_فرآيند.PDF
مقاله_بررسي_تأثير_نسبت_مولي_آلومينيم_به_تيتانيم_درپليمريزاسيون_اتي.pdf
مقاله_بررسي_تأثير_پايدارکننده_ها_و_روان_کننده_ها_برروي_ميزان_فيوژن.pdf
مقاله_بررسي_تاثير_پارامترهاي_موثر_بر_تغيير_رنگ_شربتگلوکز_در_حين_نگ.pdf
مقاله_بررسي_توليد_فيبر_خوراكي_از_تفاله_صنايع.PDF
مقاله_بررسي_جذب_بيولوژيكي_جهت_جداسازي_فلزاتسنگين_از_پسابها-_مو_(1).pdf
مقاله_بررسي_جذب_بيولوژيكي_جهت_جداسازي_فلزاتسنگين_از_پسابها-_مورد_د.pdf
مقاله_بررسي_خواص_فيزيكي_و_مكانيكي_سيستم_گل_رس.pdf
مقاله_بررسي_سينتيك_واكنش_پليمريزاسيون_راديكاليدر_حضور_آغازگر_(MMA).pdf
مقاله_بررسي_عملکرد_وينيل_تري_متوکسي_سيلان_دربهبود_چسبندگي_روکشهاي_.pdf
مقاله_بررسي_عوامل_مؤثر_در_توليد_نانوذرات.pdf
مقاله_بررسي_فرايند_احياي_سولفات_باريم_به_روش_طراحي.pdf
مقاله_بررسي_مقاومت_به_تركزايي_تنشي_محيطي.PDF
مقاله_بررسي_مقاومت_روغني_و_حرارتي_و_سينتيك_نفوذNBRCR_و_آلياژ_CR_،N.pdf
مقاله_بررسي_مكانيزم_انتقال_به_هوا_در_فرايند_حذفبيولوژيكي_اتيل_بنزن.pdf
مقاله_بررسي_ميزان_اتصال_متوكسي_پلي_اتيلن_گليكولفعال_شده_به_سطح_سلو.pdf
مقاله_بررسي_هيدروژل_هاي_حساس_به_دماي_زيستتخريب_پذير_با_پايه_كيتوسا.pdf
مقاله_بررسي_و_آناليز_عناصر_فلزي_سنگين_در_آبهايو_ppb_آشاميدني_مناطق.pdf
مقاله_بررسي_و_بهينه_سازي_اثرات_متقابل_ضريباصطكاك،_چسبندگي_و_چاپ_پذ.pdf
مقاله_بررسي_و_طراحي_سيستم_مناسب_جلوگيري_ازپلي_اتيلن_HD_انتشار_غبار.pdf
مقاله_بررسي_و_مطالعه_حلاليت_دي_اكسيد_كربن_در_حلا_لهاي_آلي_در_دماها.pdf
مقاله_بررسي_وتعيين_خواص_فيزيكي_آب_پنير_جهتاستفاده_در_طراحي_واحدهاي.pdf
مقاله_بررسي_پارامتر_هاي_عملياتي_بر_ثابت_سرعتوسينتيك_خشك_كردن_سيب.pdf
مقاله_بررسي_پتانسيل_اسيدهاي_آمينه_بعنوان_تنها_منبعكربن_و_نيتروژن_د.pdf
مقاله_بررسی_اثر_تغلیظ_اکسیژن_هوا.PDF
مقاله_بررسی_سطح_جذبی_هیدرو_کربنها.PDF
مقاله_بررسی_مکانيزم_انتقال_جرم_در_حين_تشکيل_قطره.PDF
مقاله_بكارگيري_روش_طراحي_آزمايش_تاگوچي_جهتبهينه_سازي_شرايط_رنگبري_.pdf
مقاله_بهينه_سازي_ساختارهاي_ساندويچي_بكار_رفته_در_هوا_فضا.pdf
مقاله_بهينه_سازي_شرايط_عملياتي_سيستم_لجن_فعال_و.pdf
مقاله_بيوتكنولوژي_راهكاري_براي_حذف_تركيبات_مزاحمنيتروژني_از_خوراك_.pdf
مقاله_بيوهيدرومتالورژي_انتخابي_برتر_در_اقتصاد.pdf
مقاله_تأثير_جيبرليك_اسيد_و_سبوس_برنج_بر_توليد_اتانولز_ملاس_و_شربت_.pdf
مقاله_تاثير_آمونياک_بر_گرانولاسيون_لجن_بي_هوازي.pdf
مقاله_تاثير_دما_در_بهينه_سازي_مرحله_تخمير_اكسيداتيودر_فرآيند_توليد.pdf
مقاله_تاثير_روشهاي_مختلف_فرآوري_روي_پايداري_حالتابري_آب_هويج.pdf
مقاله_تاثير_متغيرهاي_عملياتي(شدت_جريان_فازها_وشدت_ضربان)_و_انتقال_.pdf
مقاله_تاثير_مقدار_زيركونيم_روي_عملكرد_كاتاليست_كبالت.pdf
مقاله_تاثير_منبع_کربن_و_نيتروژن_بر_عملکرد_فنوکارئت_کرايزسپريوم_در_.pdf
مقاله_تاثيراستفاده_همزمان_از_دو_آغازگربروزن_مولكولي.pdf
مقاله_تبديل_مستقيم_دی_اکسيد_کربن_دردماي_پائين.PDF
مقاله_تبيين_روشي_جديد_در_فرايند_هيدروليز_متيل.pdf
مقاله_تحليل_رياضي_و_تجربي_بيوراکتور_بستر_ثابت_گلوکزايزومراز_تثبيت_.pdf
مقاله_تخريب_پذير_نمودن_زيست_محيطي_پلي_اتيلن.pdf
مقاله_ترمودینامیک_سطح_محلول_های_پلیمری.PDF
مقاله_تصفيه_آب_نمك_چرخشي_در_كارخانة_توليد_نمكجهت_كاهش_املاح_كلسيم_.pdf
مقاله_تصفيه_الكتروشيميايي_پسابهاي_رنگي_در_محيط_آبي_وبررسي_اثر_ولتا.pdf
مقاله_تعيين_شرايط_بهينه_توليد_بيوسورفكتانت_ها_بهمنظور_استفاده_در_ت.pdf
مقاله_تعيين_ميزان_لاستيك_مقيد_به_عنوان_معياري_ازبا_آلياژ_هاي_N_و_6.pdf
***سنتز p-نیترو آنیلین دانلود
***سنتز p- نیترو استانیلید دانلود
***سنتز استیل سالیسیلیک اسید(آسپرین) دانلود
***سنتز دی بنزال استون با تراکم آلدولی دانلود
سنتز آدي پيك اسيد دانلود
مجموعه گزارشکارهای آزمایشگاه شیمی آلی 2
کامل به همراه محاسباتوپاسخ سوالات
astanilid.
banzo hydrol.
adepic asid. *
asprin *
capro va diazotitasion. *
kanizaro_aldoli *
sabon. *
siclo oxim va isomerizasion *
لینک دانلود:
پسوردفایل:
مجموعه گزارشکارهای تجزیه۲ بانمودار و محاسبات وپاسخ سوالات
لینک دانلود:
پسوردفایل ها:
نويسنده : کامران مومن زاده
گزارشکارهای کامل آزمایشگاه تجزیه۱به همراه محاسبات واستوکیومتری
تيتراسيون اسيد و باز
تيتراسيون هاي رسوبي (موهر)
تيتراسيون هاي اکسايش و کاهش
اندازه گيري يون کلسيم و منيزيم و سختي آب
PH متري
هدايت سنجي
پتانسيومتري
لینک دانلود:
http://s1.picofile.com/file/7507876769/%D8%A2%D8%B2_%D8%AA%D8%AC%D8%B2%DB%8C%D9%87_1.rar.html
پسورد تمامی فایل ها:
مجموعه گزارشکارهای آزمایشگاه شیمی فیزیک 2 کامل به همراه محاسباتوپاسخ سوالات ونمودار
جذب گازها و دفع آنها
تعيين درجه واکنش
تعيين درجه واکنش
تعيين ثابت هيدروليز هيدروکلريد آنالين به روش pHm
تعيين ثابت تفکيک اسيدي اسيد استيک به روش هدايت سنجي
اندازه گيري ويسکوزيته
تععين حاصلضرب حلاليت
حجم مولي جزئي
کشش سطحي
سينيتيک واکنشهاي يوني در محلول
ضريب شکست
لینک دانلود:
پسوردفایل:
مجموعه گزارشکارهای آزمایشگاه شیمی فیزیک 1 کامل به همراه محاسباتوپاسخ سوالات
لینک دانلودمستقیم
پسوردفایل:
کارشناس آزمایشگاه:
نويسنده : کامران مومن زاده
استاد : دکتر رحیمی
این آزمایشگاه مربوط به رشته های فنی مهندسی و علوم پایه است.
در این آزمایشگاه آزمایشهای زیر انجام می گیرد
آزمایشگاه شیمی تجزیه 1
جلسه 1: محلول سازی
جلسه 2: آزمایش اسیدیمتری
جلسه 3: آزمایش آلکالیمتری
جلسه 8: آزمایش اندازه گیری نیکل توسط دی متیل گلی اکسایم (تجزیه وزنی)
جلسه 9: آزمایش تیتراسیون کمپلکسومتری برگشتی اندازه گیری نیکل
جهت دانلود فایل کامل دستور کار روی عنوان آزمایشگاه کلیک نمایید.
نام و نام خانوادگی: کامران مومن زاده
استاد : دکتر قربانی
این آزمایشگاه مربوط به رشته های فنی مهندسی و علوم پایه است.
در این آزمایشگاه آزمایشهای زیر انجام می گیرد:
آزمایشگاه شیمی آلی 1
جلسه 1: اندازه گیری نقطه ذوب
جلسه 2: اندازه گیری نقطه جوش
جلسه 3: کروماتوگرافی
جلسه 4: تبلور مجدد
جلسه 5: استخراج
جلسه 6: آنالیز کیفی ترکیبات آلی ( شناسایی نیتروژن و هالوژن ها)
جلسه 7: تقطیر
جهت دانلود فایل کامل دستور کار روی عنوان آزمایشگاه کلیک نمایید.
تیوسولفات سدیم نمک اسید تیو سولفوریک می باشد که این اسید بر خلاف نمک هایش بسیار ناپایدار است. اگر به محلول تیوسولفات سدیم محلول یک اسید قوی مثل اسید کلریدریک افزوده شود پس از اندک مدتی گوگرد رسوب نموده و محلول شدیدا بوی انیدرید سولفورو می دهد.
تیوسولفات سدیم به آسانی کلر را احیا می نماید.
Na2SO3 + H2O + Cl2 → Na2SO4 +۲HCl + S
اگر مقدار کلر زیاد باشد عدد اکسایش گوگرد از ۲- به ۶+ می رسد.
Na2SO3 + 5H2O + 4Cl2 → ۲Na2HSO4 + 8HCl
برای مطالعه ادامه گزارش کار و روش تهیه تیو سولفات سدیم به ادامه مطلب بروید.
در عکاسی سدیم تیوسولفات به عنوان داروی ثبوت مصرف می گردد. زیرا تیوسولفات بر هالوژن های نقره اثر کرده و به آسانی انها را حل می نماید ولی بر خود نقره بی اثر است.
AgCl +2Na2SO3 → Na3[Ag(S2O3)2] + NaCl
در شیمی تجزیه واکنش بین تیوسولفات و ید اساس سنجش های یدومتری می باشد.
برای تهیه نمک تیوسولفات می توان از سولفیت سدیم و گل گوگرد استفاده نمود. اگر سولفیت سدیم در دسترس نباشد می توان ان را از اثر گاز SO2 بر کربنات سدیم بدست اورد. گاز SO2 از اثر اسید سولفوریک غلیظ بر پودر مس تهیه می گردد.
دستگاهی مطابق شکل زیر سوار کنید و نمک سولفیت سدیم را تهیه نمایید. سرعت خروج گاز SO2 را می توان توسط شعله و میزان اسید سولفوریک غلیظ کنترول نمود.
مواد مورد نیاز:
سولفیت سدیم ، گوگرد ، آب مقطر ، بشر ۳۰۰ میلی لیتری ، ترازو ، هیتر ، قیف ، کاغذ صافی ، ارلن
روش تهیه :
ابتدا ۶ گرم سولفیت سدیم را همراه با ۳۰ میلی لیتر آب مقطر در یک بشر ۳۰۰ میلی لیتری وارد نموده و تا نقطه جوش حرارت دهید تا حل گردد. ۲ گرم گوگرد اضافه نموده و محلول تعلیقی حاصل را بجوشانید تا تقریبا تمام گوگرد وارد واکنش شود. محصول را تا داغ است صاف کنید. محلول زیر صافی را تبخیر نموده تا تبلور شروع شود. سپس در حمام یخ سرد نموده و توسط پمپ خلا صاف نمایید. ماده بدست امده را در یک اون در دمای ۴۰ تا ۵۰ درجه سانتیگراد خشک نمایید.
تعیین آب تبلور محصول بدست آمده :
۲٫۴۸ گرم از نمک بدست امده را در اب مقطر حل نموده و به حجم ۱۰۰ میلی لیتر برسانید و انرا توسط محلول استاندارد تیتر نمایید. برای تهیه محلول استاندارد ۱٫۲۷ گرم ید و ۱ گرم یدور پتاسیم را همراه با اب مقطر در بالن ژوژه ۱۰۰ میلی لیتری وارد نموده و با اضافه نمودن اب مقطر بعد از انحلال کامل ان را به حجم برسانید. ۱۰ میلی لیتر از محلول نمک بدست امده را در مجاورت چسب نشاسته با محلول استاندارد تیتر نمایید.
برای دانلود گزارش کار آزمایشگاهی روش تهیه و استاندارد کردن سدیم تیو سولفات ۰٫۱ مولار به ادامه مطلب بروید.
نام فایل : Preparation and standardization of 0.1 M Na2S2O3
نوع فایل : pdf
حجم فایل : ۲۵۷ کیلوبایت
رمز عبور : ندارد
لینک دانلود : دانلود
استاد : دکتر رحیمی
نويسنده : کامران مومن زاده
نام آزمایش: تعیین میزان آهن آرد به روش اسپکتروفتومتری
هدف آزمایش:
دامنه کاربرد: این روش برای اندازه گیری آهن درغلات و آردهای حاصل از آنها – آردهای غنی شده و آماده شده برای پخت و فرآوردههای آنها کاربرد دارد.
وسائل و مواد آزمایش:
خاکستر آرد- اسید کلریدریک – بن ماری – آزیتاتور- کاغذ صافی- بالن ژوژه- محلول استاندارد آهن – محلول هیروکسیل آمین – محلول تامپون استات
محلول ارتوفنانترولین
تئوری آزمایش:
عنوان: اسپکتروفتومتری
هدف: آشنایی با دستگاه اسپکتروفتومتر
تئوری: اسپکتروفتومتر ناحیه مریی Spectrophotometer
تعریف اسپکتروفتومتری:
اسپکتروفتومتری یک روش تجزیه دستگاهی است که در آن تابش الکترومغناطیسی در ناحیه مرئی و ماورا بنفش جذب ماده میشود، و از روی شدت جذب مقدار ماده تعیین میشود.
نام آزمایش
تیتراسیون آهن (II) با سریم (IV)
عنوان
تیتراسیون آهن (II) با سریم (IV)
هدف
اندازه گیری درصد آهن در یک ترکیب از طریق تیتراسیون پتانسیومتری آهن (II ) با محلول استاندارد سریک آمونیوم نیترات
مواد لازم
تیتر شونده: آهن (II ) با غلظت 0.1 مولار
تیتر کننده: محلول 0.1 مولار سریک آمونیوم نیترات
وسايل لازم
مگنت ، بشر ، بالن ژوژه ، پیپت حبابدار ، بورت،پایه بورت،همزن مغناطیسی،الکترود شناساگر پلاتین،الکترود مرجع
تئوری :
به معناي سنجش و اندازه گيري پتانسيل است. در شاخه اي از شيمي به نام الكتروشيمي ، بحث از پيل الكتروشيميايي است. پيل الكتروشيميايي دستگاهي است كه انرژي واكنش شيميايي را كه در شرايط معمولي اغلب به صورت انرژي گرمايي آزاد مي شود، به انرژي الكتريكي قابل استفاده تبديل مي نمايد و مانند سدهاي هيدروالكتريك، مانع از به هدر رفتن انرژي مي شود. دو الكترود و يك پل نمكي ، تشكيل يك پيل را مي دهند. درواقع دو الكترود به دليل رقابت براي تبادل الكترون، تمايل متفاوت براي گرفتن الكترون دارند و اين تفاوت گرفتن الكترون، در شرايط مناسب سبب انتقال الكتريسيته مي شود. اين جريان الكتريسيته داراي يك ولتاژ يا پتانسيل خاص مي باشد كه با دستگاه ولت سنج قابل اندازه گيري است.
نويسنده : کامران مومن زاده
تئوری آزمایش:
پیوندهای شیمیایی اسید سیتریک
اسید استیک یا جوهر انگور جز اسیدهای کربوکسیلیک است و در نامگذاری آیوپاک به اسید اتانوئیک معروف است.
نگاه کلی اسید استیک جز اسیدهای کربوکسیلیک میباشد و در نامگذاری آیوپاک به اسید اتانوئیک معروف است. این اسید دارای فرمول شیمیایی میباشد و در قسمت چشایی طعم ترشی ، شبیه طعم سرکه میدهد.
باکتریهای مخمر سرکه به دلیل تمایل به تولید اسید استیک به این نام معروف شدهاند. این باکتریها در مواد غذایی ، آب و خاک یافت میشوند. اسید استیک بطور طبیعی از میوهها و برخی مواد غذایی فاسد شده از فرایند تخمیر تولید میشوند و از قدیمیترین ترکیبات شیمیایی شناخته شده توسط انسان میباشد. تاریخچه سرکه (اسید استیک رقیق) از دوران باستان برای انسان شناخته شده بود. احتمالاً انسانها در دوران باستان هنگام تهیه شراب از فرایند تخمیر به وجود سرکه پی برده بودند. فیلسوف یونانی تئوفاراستوس در سه قرن پیش از میلاد چگونگی واکنش سرکه با فلزات و تولید رنگدانه برای استفاده در نقاشی از کربنات سرب و زاجهای سبز ایجاد شده از نمکهای مس و استات مس را توضیح دادهاست. رومیان باستان با نگهداری شراب ترش در قدحهای سربی ، شراب بسیار شیرینی به نام Sapa تولید میکردند که طعم شیرین آن ناشی از استات سرب بودهاست که امروزه دانشمندان مرگ زودرس بسیاری از اشراف روم را به مسمومیت ناشی از این ماده نسبت دادهاند. شیمیدانهای عصر رنسانس اسید استیک گلاسیال (منجمد) را از تقطیر خشک استاتهای فلزی تهیه میکردند. در سال ۱۸۴۷ هرمن کولب شیمیدان آلمانی برای اولین بار اسید استیک را از مواد معدنی سنتز کرد. خواص اسید استیک خالص، مایعی بیرنگ با بویی تیز، مایعی خورنده و قابل اشتعال میباشد. این اسید در ۱۶٫۶ درجه سانتیگراد منجمد میشود. به این دلیل و همچنین ظاهر یخ مانند آن به نام اسید استیک گلاسیال معروف است. اسید استیک در محلولهای آبی میتواند تفکیک شده و یون استات تولید کند. PH آن برابر با ۴٫۸ میباشد، یعنی در PH=۴٫۸ نیمی از مولکولهای اسید استیک در محلول آبی به صورت یون استات هستند. اسید استیک در حالت بخار شامل دیمرهایی از دو مولکول اسید استیک میباشد که با پیوند هیدروژنی با یکدیگر ارتباط دارند.
عنوان : ازمایش اندازه گیری انرژی اکتیواسیون
هدف : اندازه گیری انرژی اکتیواسیون
تئوري آزمايش :
انرژي اكتيواسيون يكي از پارامترهاي در انجام واكنش هاي شيميايي است.
اثر دما بر ثابت سرعت واكنش به صورت زير خواهد بود :
اگر از طرفين رابطة فوق Ln بگيريم ، رابطه به صورت زير ساده مي شود
در دو دماي مختلف مقدار K به صورت زير خواهد بود :
از تفاضل دو رابطة بالا داريم
موضوع آزمايش: اندازه گيري انرژي اكتيواسيون
شرح آزمايش :
ابتدا محلول استات اتيل و محلول سود بسازيد.
از هر يك از اين محلول ها برداشته و به حجم برسانيد .
هدايت هر يك از اين محلول ها را به وسيلة كنداكتومتر اندازه بگيريد . (محلول سود را و محلول استات سديم را در نظر مي گيريم )
سپس از هر يك از اين محلول ها را برداشته و با هم مخلوط مي كنيم ، ميزان هدايت را در زمان هاي مختلف يادداشت مي كنيم .
اين آزمايش را در دو دماي انجام مي دهيم .
نتايج و محاسبات انجام شده :
1 7 6.74 -44.58
2 14 6.09 -10.86
3 21 5.56 -7.04
4 28 5.29 -6.05
5 35 5.03 -5.36
6 42 4.78 -4.85
1 7 8.69 -6.08
2 14 7.32 -3.89
3 21 6.69 -3.41
4 28 6.27 -3.17
5 35 5.71 -2.92
6 42 5.61 -2.88
این متن ناقص است برای مشاهده متن کامل آن را دانلود نمایید.
در صورت خراب بودن لینک دانلود " در قسمت نظر دهید " به ما اطلاع دهید تا مشکل را رفع کنیم
حجم فایل : 50 کیلو بایت | فرمت فایل : Docx | زبان : فارسی
دانلود مستقیم | پسورد فایل : kimiagari.ir
 گزارشکار آزمایشگاه شیمی صنعتی
گزارشکار آزمایشگاه شیمی صنعتی گزارش کار شیمی عمومی2 شناسایی و جداسازی کاتیون های گروه چهارم
گزارش کار شیمی عمومی2 شناسایی و جداسازی کاتیون های گروه چهارم نام آزمایش : تهیه پتاسیم تري اگزالاتو کرومات (III) تري هيدرات
نام آزمایش : تهیه پتاسیم تري اگزالاتو کرومات (III) تري هيدرات آزمایشگاه بیوشیمی1
آزمایشگاه بیوشیمی1 گزارشکار تعیین درصد خلوص مواد شیمیایی
گزارشکار تعیین درصد خلوص مواد شیمیایی دانلود جزوه شیمی عمومی 1
دانلود جزوه شیمی عمومی 1 اتیلن دی آمین تترا استیک اسید (Ethylenediaminetetraacetic acid) (EDTA)
اتیلن دی آمین تترا استیک اسید (Ethylenediaminetetraacetic acid) (EDTA) گزارشکار آزمایشگاه فیزیولوژی جانوری
گزارشکار آزمایشگاه فیزیولوژی جانوری محلول های بافر یا تامپون
محلول های بافر یا تامپون متیل اورانژ چیست و چگونه تشکیل می شود؟
متیل اورانژ چیست و چگونه تشکیل می شود؟ قیف بوخنر و ارلن خلاء (ارلن تصفیه) (ارلن تخلیه) ( Buchner Funnel & Filter Flask)
قیف بوخنر و ارلن خلاء (ارلن تصفیه) (ارلن تخلیه) ( Buchner Funnel & Filter Flask) استوانه مدرج (Graduated Cylinder)
استوانه مدرج (Graduated Cylinder) ایمنی و کمکهای اولیه در آزمایشگاه شیمی
ایمنی و کمکهای اولیه در آزمایشگاه شیمی تاریخچه عناصر شیمیایی
تاریخچه عناصر شیمیایی ضریب شکست نور
ضریب شکست نور تاثیر پلاستیک بر سلامت
تاثیر پلاستیک بر سلامت ديوكسين پايدارترين سم در محيط زيست
ديوكسين پايدارترين سم در محيط زيست آنیون ها و کاتیون ها
آنیون ها و کاتیون ها انیمشن جالب تعاملی آزمایش رادرفورد
انیمشن جالب تعاملی آزمایش رادرفورد کتاب گزارش کار شیمی عمومی
کتاب گزارش کار شیمی عمومی