دانلود پایان نامه کارشناسی ارشد تجزیه
سایت شیمیست ایرانی پس از مدتها تلاش پایان نامه ی "اندازه گیری همزمان گونه ها بوسیله ی انالیز کمومتریکس داده های تیتراسیون های پتانسیل سنجی و اسپکتروفتومتری"را برای شما عزیزان و پژوهشگران گرانقدر فراهم آورده است.دانلود کنید و لذت ببرید.
دانلود فایل رمز فایل:www.analyte.ir
این مطلب در تاریخ: چهار شنبه 11 دی 1392 ساعت: 6:15 منتشر شده است
برچسب ها : دانلود پایان نامه کارشناسی ارشد تجزیه,
مقاله شیمی
مقاله_-_L_مطالعه_تخريب_حرارتي_در_سنتز_پليلاكتايد_به_روش_پليمر_شدن_.pdf
مقاله_Aspergillus_بررسي_توليد_لواستاتين_از_سويه.pdf
مقاله_GM-CSF_بهينه_سازي_توليد_ترشحی.PDF
مقاله_SCP_بررسی_وضعيت_توليد_و_مصرف.PDF
مقاله_آماده_سازي_و_ويژگي_هاي_لومينسنس_يك_فسفر.pdf
مقاله_اثر_متغيرهاي_فرآيند_پرتودهي_روي_استحكامبه_UHMWPE_PET_كششي_و_.pdf
مقاله_ارائه_روش_موثر_جهت_بازيابي_و_جلوگيري_از_دور_ريز.pdf
مقاله_ارزيابي_عملکرد_باکتريهای_جداسازی_شده_از_مخاز_ن.PDF
مقاله_ارزيابي_نحوه_و_روند_انتشار_آلاينده_هاي_هوا_در.pdf
مقاله_از_آب_و_خاك_آلوده_MTBE_روشهاي_حذف.pdf
مقاله_از_باگاس_نيشكر_(_Biooil_)_توليد_زيست_سوخت.pdf
مقاله_ازمنابع_آب_MTBE_بررسي_حذف_ماده_آلاينده.pdf
مقاله_استفاده_از_تكنولوژي_آنزيم_در_فرآوري_خمير.pdf
مقاله_استفاده_از_روش_افزايش_بيولوژيکي_در_تصفيهپساب_کارخانجات_لبنيا.pdf
مقاله_استفاده_از_شروع_كننده_هاي_دو_عاملي_درپليمريزاسيون_راديكالي.pdf
مقاله_اصلاح_خواص_فيزيكي_و_مكانيكي_سيستم_هاي_برپايه_گل_رس_با_استفاد.pdf
مقاله_اصلاح_شيميايي_ساختار_پليمر_ليفياكريلونيتريل_با_استفاده_از_تر.pdf
مقاله_اصلاح_شيميايي_ساختار_پليمر_ليفياكريلونيتريل_با_استفاده_از_تر.pdf
مقاله_اصلاح_پليمري_كامپوزيت_هاي_بر_پايه_گل_رس.pdf
مقاله_اصلاح_چسبندگي_پلي_يورتان_به_سيليكون_رابر.pdf
مقاله_انتخاب_مدلهاي_سينتيكي_مناسب_براي_بررسي_رشد.pdf
مقاله_اندازه_گيری_غلظت_سلولی_و_تعيين_کيفيت_آن.PDF
مقاله_اولوي_تهاي_بهر_هگيري_از_نانوفناوري.PDF
مقاله_بازده_حذف_بنزن_در_پسابهاي_پتروشيمي_با_فرآيند.pdf
مقاله_بازيابي_آب_كلردار_واحد_كلرآلكالي_شركت_كيميايپتروشيمي_بندراما.pdf
مقاله_بازيابي_پلاتين_از_كاتاليزورهاي_مستعمل_واحد_ريفورمينگ.pdf
مقاله_بر_مورفولوژي_و_(_PVP_)_اثر_پلي_وينيل_پيروليدونغشاء_(_Support.pdf
مقاله_بررسي_آميزه_پلي_وينيل_کلرايد_اکريلونيتريلجهت_تهيه_کاغذ_(PVCN.pdf
مقاله_بررسي_اثر_پارامتر_هاي_مختلف_بر_پليمريزاسيونبه_روش_طراحي_THT_.pdf
مقاله_بررسي_اثرشوك_حرارتي_برروي_پروتئين_تك_ياختهاز_آب_پنير.pdf
مقاله_بررسي_احتمال_تغيير_جرم_مولكولي_متوسط_وزنييك_نمونه_پلي_اكسي_ا.pdf
مقاله_بررسي_ايزومري_شدن_آنزيمي_گلوكز_به_فروكتوز_دريك_جت_راكتور_با_.pdf
مقاله_بررسي_تأثير_فرمولاسيون_و_شرايط_فرآيند.PDF
مقاله_بررسي_تأثير_نسبت_مولي_آلومينيم_به_تيتانيم_درپليمريزاسيون_اتي.pdf
مقاله_بررسي_تأثير_پايدارکننده_ها_و_روان_کننده_ها_برروي_ميزان_فيوژن.pdf
مقاله_بررسي_تاثير_پارامترهاي_موثر_بر_تغيير_رنگ_شربتگلوکز_در_حين_نگ.pdf
مقاله_بررسي_توليد_فيبر_خوراكي_از_تفاله_صنايع.PDF
مقاله_بررسي_جذب_بيولوژيكي_جهت_جداسازي_فلزاتسنگين_از_پسابها-_مو_(1).pdf
مقاله_بررسي_جذب_بيولوژيكي_جهت_جداسازي_فلزاتسنگين_از_پسابها-_مورد_د.pdf
مقاله_بررسي_خواص_فيزيكي_و_مكانيكي_سيستم_گل_رس.pdf
مقاله_بررسي_سينتيك_واكنش_پليمريزاسيون_راديكاليدر_حضور_آغازگر_(MMA).pdf
مقاله_بررسي_عملکرد_وينيل_تري_متوکسي_سيلان_دربهبود_چسبندگي_روکشهاي_.pdf
مقاله_بررسي_عوامل_مؤثر_در_توليد_نانوذرات.pdf
مقاله_بررسي_فرايند_احياي_سولفات_باريم_به_روش_طراحي.pdf
مقاله_بررسي_مقاومت_به_تركزايي_تنشي_محيطي.PDF
مقاله_بررسي_مقاومت_روغني_و_حرارتي_و_سينتيك_نفوذNBRCR_و_آلياژ_CR_،N.pdf
مقاله_بررسي_مكانيزم_انتقال_به_هوا_در_فرايند_حذفبيولوژيكي_اتيل_بنزن.pdf
مقاله_بررسي_ميزان_اتصال_متوكسي_پلي_اتيلن_گليكولفعال_شده_به_سطح_سلو.pdf
مقاله_بررسي_هيدروژل_هاي_حساس_به_دماي_زيستتخريب_پذير_با_پايه_كيتوسا.pdf
مقاله_بررسي_و_آناليز_عناصر_فلزي_سنگين_در_آبهايو_ppb_آشاميدني_مناطق.pdf
مقاله_بررسي_و_بهينه_سازي_اثرات_متقابل_ضريباصطكاك،_چسبندگي_و_چاپ_پذ.pdf
مقاله_بررسي_و_طراحي_سيستم_مناسب_جلوگيري_ازپلي_اتيلن_HD_انتشار_غبار.pdf
مقاله_بررسي_و_مطالعه_حلاليت_دي_اكسيد_كربن_در_حلا_لهاي_آلي_در_دماها.pdf
مقاله_بررسي_وتعيين_خواص_فيزيكي_آب_پنير_جهتاستفاده_در_طراحي_واحدهاي.pdf
مقاله_بررسي_پارامتر_هاي_عملياتي_بر_ثابت_سرعتوسينتيك_خشك_كردن_سيب.pdf
مقاله_بررسي_پتانسيل_اسيدهاي_آمينه_بعنوان_تنها_منبعكربن_و_نيتروژن_د.pdf
مقاله_بررسی_اثر_تغلیظ_اکسیژن_هوا.PDF
مقاله_بررسی_سطح_جذبی_هیدرو_کربنها.PDF
مقاله_بررسی_مکانيزم_انتقال_جرم_در_حين_تشکيل_قطره.PDF
مقاله_بكارگيري_روش_طراحي_آزمايش_تاگوچي_جهتبهينه_سازي_شرايط_رنگبري_.pdf
مقاله_بهينه_سازي_ساختارهاي_ساندويچي_بكار_رفته_در_هوا_فضا.pdf
مقاله_بهينه_سازي_شرايط_عملياتي_سيستم_لجن_فعال_و.pdf
مقاله_بيوتكنولوژي_راهكاري_براي_حذف_تركيبات_مزاحمنيتروژني_از_خوراك_.pdf
مقاله_بيوهيدرومتالورژي_انتخابي_برتر_در_اقتصاد.pdf
مقاله_تأثير_جيبرليك_اسيد_و_سبوس_برنج_بر_توليد_اتانولز_ملاس_و_شربت_.pdf
مقاله_تاثير_آمونياک_بر_گرانولاسيون_لجن_بي_هوازي.pdf
مقاله_تاثير_دما_در_بهينه_سازي_مرحله_تخمير_اكسيداتيودر_فرآيند_توليد.pdf
مقاله_تاثير_روشهاي_مختلف_فرآوري_روي_پايداري_حالتابري_آب_هويج.pdf
مقاله_تاثير_متغيرهاي_عملياتي(شدت_جريان_فازها_وشدت_ضربان)_و_انتقال_.pdf
مقاله_تاثير_مقدار_زيركونيم_روي_عملكرد_كاتاليست_كبالت.pdf
مقاله_تاثير_منبع_کربن_و_نيتروژن_بر_عملکرد_فنوکارئت_کرايزسپريوم_در_.pdf
مقاله_تاثيراستفاده_همزمان_از_دو_آغازگربروزن_مولكولي.pdf
مقاله_تبديل_مستقيم_دی_اکسيد_کربن_دردماي_پائين.PDF
مقاله_تبيين_روشي_جديد_در_فرايند_هيدروليز_متيل.pdf
مقاله_تحليل_رياضي_و_تجربي_بيوراکتور_بستر_ثابت_گلوکزايزومراز_تثبيت_.pdf
مقاله_تخريب_پذير_نمودن_زيست_محيطي_پلي_اتيلن.pdf
مقاله_ترمودینامیک_سطح_محلول_های_پلیمری.PDF
مقاله_تصفيه_آب_نمك_چرخشي_در_كارخانة_توليد_نمكجهت_كاهش_املاح_كلسيم_.pdf
مقاله_تصفيه_الكتروشيميايي_پسابهاي_رنگي_در_محيط_آبي_وبررسي_اثر_ولتا.pdf
مقاله_تعيين_شرايط_بهينه_توليد_بيوسورفكتانت_ها_بهمنظور_استفاده_در_ت.pdf
مقاله_تعيين_ميزان_لاستيك_مقيد_به_عنوان_معياري_ازبا_آلياژ_هاي_N_و_6.pdf
این مطلب در تاریخ: چهار شنبه 11 دی 1392 ساعت: 5:7 منتشر شده است
برچسب ها : مقاله شیمی,
گزارش کار آزمایشگاه شیمی آلی 2
***سنتز p-نیترو آنیلین دانلود
***سنتز p- نیترو استانیلید دانلود
***سنتز استیل سالیسیلیک اسید(آسپرین) دانلود
***سنتز دی بنزال استون با تراکم آلدولی دانلود
سنتز آدي پيك اسيد دانلود
این مطلب در تاریخ: چهار شنبه 11 دی 1392 ساعت: 3:55 منتشر شده است
برچسب ها : گزارش کار آزمایشگاه شیمی آلی 2 ,
پاور پوینت تمام آزمایش های شیمی معدنی ۱
این مطلب در تاریخ: دو شنبه 9 دی 1392 ساعت: 23:43 منتشر شده است
برچسب ها : پاور پوینت تمام آزمایش های شیمی معدنی ۱,
گزارشکار شیمی معدنی تهیه رنگدانه
این مطلب در تاریخ: دو شنبه 9 دی 1392 ساعت: 23:40 منتشر شده است
برچسب ها : گزارشکار شیمی معدنی تهیه رنگدانه,
گزارشکار آزمایشگاه شیمی صنعتی
گزارشکار آزمایشگاه شیمی معدنی ۱
دانلود گزارشکار آزمایشگاه شیمی فیزیک ۱
دانلود گزارشکار آزمایشگاه شیمی آلی ۲
آزمایشگاه شیمی آلی 2
مجموعه گزارشکارهای آزمایشگاه شیمی آلی 2
کامل به همراه محاسباتوپاسخ سوالات
astanilid.
banzo hydrol.
adepic asid. *
asprin *
capro va diazotitasion. *
kanizaro_aldoli *
sabon. *
siclo oxim va isomerizasion *
لینک دانلود:
پسوردفایل:
این مطلب در تاریخ: یک شنبه 1 دی 1392 ساعت: 1:57 منتشر شده است
آزمایشگاه شیمی آلی 1
آزمایشگاه تجزیه 2
مجموعه گزارشکارهای تجزیه۲ بانمودار و محاسبات وپاسخ سوالات
لینک دانلود:
پسوردفایل ها:
این مطلب در تاریخ: یک شنبه 1 دی 1392 ساعت: 1:52 منتشر شده است
برچسب ها : آزمایشگاه تجزیه 2,
آزمایشگاه تجزیه 1
نويسنده : کامران مومن زاده
گزارشکارهای کامل آزمایشگاه تجزیه۱به همراه محاسبات واستوکیومتری
تيتراسيون اسيد و باز
تيتراسيون هاي رسوبي (موهر)
تيتراسيون هاي اکسايش و کاهش
اندازه گيري يون کلسيم و منيزيم و سختي آب
PH متري
هدايت سنجي
پتانسيومتري
لینک دانلود:
http://s1.picofile.com/file/7507876769/%D8%A2%D8%B2_%D8%AA%D8%AC%D8%B2%DB%8C%D9%87_1.rar.html
پسورد تمامی فایل ها:
این مطلب در تاریخ: یک شنبه 1 دی 1392 ساعت: 1:49 منتشر شده است
برچسب ها : آزمایشگاه تجزیه 1,
آزمایشگاه شیمی فیزیک 2
مجموعه گزارشکارهای آزمایشگاه شیمی فیزیک 2 کامل به همراه محاسباتوپاسخ سوالات ونمودار
جذب گازها و دفع آنها
تعيين درجه واکنش
تعيين درجه واکنش
تعيين ثابت هيدروليز هيدروکلريد آنالين به روش pHm
تعيين ثابت تفکيک اسيدي اسيد استيک به روش هدايت سنجي
اندازه گيري ويسکوزيته
تععين حاصلضرب حلاليت
حجم مولي جزئي
کشش سطحي
سينيتيک واکنشهاي يوني در محلول
ضريب شکست
لینک دانلود:
پسوردفایل:
این مطلب در تاریخ: یک شنبه 1 دی 1392 ساعت: 1:47 منتشر شده است
برچسب ها : آزمایشگاه شیمی فیزیک 2,
آزمایشگاه شیمی فیزیک 1
مجموعه گزارشکارهای آزمایشگاه شیمی فیزیک 1 کامل به همراه محاسباتوپاسخ سوالات
لینک دانلودمستقیم
پسوردفایل:
این مطلب در تاریخ: یک شنبه 1 دی 1392 ساعت: 1:45 منتشر شده است
برچسب ها : آزمایشگاه شیمی فیزیک 1,
آزمایشگاه شیمی تجزیه
کارشناس آزمایشگاه:
نويسنده : کامران مومن زاده
استاد : دکتر رحیمی
این آزمایشگاه مربوط به رشته های فنی مهندسی و علوم پایه است.
در این آزمایشگاه آزمایشهای زیر انجام می گیرد
آزمایشگاه شیمی تجزیه 1
-
جلسه 1: محلول سازی
-
جلسه 2: آزمایش اسیدیمتری
-
جلسه 3: آزمایش آلکالیمتری
-
جلسه 8: آزمایش اندازه گیری نیکل توسط دی متیل گلی اکسایم (تجزیه وزنی)
-
جلسه 9: آزمایش تیتراسیون کمپلکسومتری برگشتی اندازه گیری نیکل
جهت دانلود فایل کامل دستور کار روی عنوان آزمایشگاه کلیک نمایید.
این مطلب در تاریخ: یک شنبه 1 دی 1392 ساعت: 1:24 منتشر شده است
برچسب ها : آزمایشگاه شیمی تجزیه,
آزمایشگاه شیمی آلی
نام و نام خانوادگی: کامران مومن زاده
استاد : دکتر قربانی
این آزمایشگاه مربوط به رشته های فنی مهندسی و علوم پایه است.
در این آزمایشگاه آزمایشهای زیر انجام می گیرد:
آزمایشگاه شیمی آلی 1
-
جلسه 1: اندازه گیری نقطه ذوب
-
جلسه 2: اندازه گیری نقطه جوش
-
جلسه 3: کروماتوگرافی
-
جلسه 4: تبلور مجدد
-
جلسه 5: استخراج
-
جلسه 6: آنالیز کیفی ترکیبات آلی ( شناسایی نیتروژن و هالوژن ها)
-
جلسه 7: تقطیر
جهت دانلود فایل کامل دستور کار روی عنوان آزمایشگاه کلیک نمایید.
این مطلب در تاریخ: یک شنبه 1 دی 1392 ساعت: 1:22 منتشر شده است
برچسب ها : آزمایشگاه شیمی آلی,
نام آزمایش: تهیه پتاسیم اگزالاتو فرات
تهیه تیوسولفات سدیم
تیوسولفات سدیم نمک اسید تیو سولفوریک می باشد که این اسید بر خلاف نمک هایش بسیار ناپایدار است. اگر به محلول تیوسولفات سدیم محلول یک اسید قوی مثل اسید کلریدریک افزوده شود پس از اندک مدتی گوگرد رسوب نموده و محلول شدیدا بوی انیدرید سولفورو می دهد.
تیوسولفات سدیم به آسانی کلر را احیا می نماید.
Na2SO3 + H2O + Cl2 → Na2SO4 +۲HCl + S
اگر مقدار کلر زیاد باشد عدد اکسایش گوگرد از ۲- به ۶+ می رسد.
Na2SO3 + 5H2O + 4Cl2 → ۲Na2HSO4 + 8HCl
برای مطالعه ادامه گزارش کار و روش تهیه تیو سولفات سدیم به ادامه مطلب بروید.
در عکاسی سدیم تیوسولفات به عنوان داروی ثبوت مصرف می گردد. زیرا تیوسولفات بر هالوژن های نقره اثر کرده و به آسانی انها را حل می نماید ولی بر خود نقره بی اثر است.
AgCl +2Na2SO3 → Na3[Ag(S2O3)2] + NaCl
در شیمی تجزیه واکنش بین تیوسولفات و ید اساس سنجش های یدومتری می باشد.
برای تهیه نمک تیوسولفات می توان از سولفیت سدیم و گل گوگرد استفاده نمود. اگر سولفیت سدیم در دسترس نباشد می توان ان را از اثر گاز SO2 بر کربنات سدیم بدست اورد. گاز SO2 از اثر اسید سولفوریک غلیظ بر پودر مس تهیه می گردد.
دستگاهی مطابق شکل زیر سوار کنید و نمک سولفیت سدیم را تهیه نمایید. سرعت خروج گاز SO2 را می توان توسط شعله و میزان اسید سولفوریک غلیظ کنترول نمود.
مواد مورد نیاز:
سولفیت سدیم ، گوگرد ، آب مقطر ، بشر ۳۰۰ میلی لیتری ، ترازو ، هیتر ، قیف ، کاغذ صافی ، ارلن
روش تهیه :
ابتدا ۶ گرم سولفیت سدیم را همراه با ۳۰ میلی لیتر آب مقطر در یک بشر ۳۰۰ میلی لیتری وارد نموده و تا نقطه جوش حرارت دهید تا حل گردد. ۲ گرم گوگرد اضافه نموده و محلول تعلیقی حاصل را بجوشانید تا تقریبا تمام گوگرد وارد واکنش شود. محصول را تا داغ است صاف کنید. محلول زیر صافی را تبخیر نموده تا تبلور شروع شود. سپس در حمام یخ سرد نموده و توسط پمپ خلا صاف نمایید. ماده بدست امده را در یک اون در دمای ۴۰ تا ۵۰ درجه سانتیگراد خشک نمایید.
تعیین آب تبلور محصول بدست آمده :
۲٫۴۸ گرم از نمک بدست امده را در اب مقطر حل نموده و به حجم ۱۰۰ میلی لیتر برسانید و انرا توسط محلول استاندارد تیتر نمایید. برای تهیه محلول استاندارد ۱٫۲۷ گرم ید و ۱ گرم یدور پتاسیم را همراه با اب مقطر در بالن ژوژه ۱۰۰ میلی لیتری وارد نموده و با اضافه نمودن اب مقطر بعد از انحلال کامل ان را به حجم برسانید. ۱۰ میلی لیتر از محلول نمک بدست امده را در مجاورت چسب نشاسته با محلول استاندارد تیتر نمایید.
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 23:20 منتشر شده است
برای دانلود گزارش کار آزمایشگاهی روش تهیه و استاندارد کردن سدیم تیو سولفات ۰٫۱ مولار به ادامه مطلب بروید.
نام فایل : Preparation and standardization of 0.1 M Na2S2O3
نوع فایل : pdf
حجم فایل : ۲۵۷ کیلوبایت
رمز عبور : ندارد
لینک دانلود : دانلود
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 23:19 منتشر شده است
تعیین میزان آهن آرد به روش اسپکتروفتومتری
استاد : دکتر رحیمی
نويسنده : کامران مومن زاده
نام آزمایش: تعیین میزان آهن آرد به روش اسپکتروفتومتری
هدف آزمایش:
دامنه کاربرد: این روش برای اندازه گیری آهن درغلات و آردهای حاصل از آنها – آردهای غنی شده و آماده شده برای پخت و فرآوردههای آنها کاربرد دارد.
وسائل و مواد آزمایش:
خاکستر آرد- اسید کلریدریک – بن ماری – آزیتاتور- کاغذ صافی- بالن ژوژه- محلول استاندارد آهن – محلول هیروکسیل آمین – محلول تامپون استات
محلول ارتوفنانترولین
تئوری آزمایش:
عنوان: اسپکتروفتومتری
هدف: آشنایی با دستگاه اسپکتروفتومتر
تئوری: اسپکتروفتومتر ناحیه مریی Spectrophotometer
تعریف اسپکتروفتومتری:
اسپکتروفتومتری یک روش تجزیه دستگاهی است که در آن تابش الکترومغناطیسی در ناحیه مرئی و ماورا بنفش جذب ماده میشود، و از روی شدت جذب مقدار ماده تعیین میشود.
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 2:3 منتشر شده است
گزارش کار اندازه گیری یون مس
هدف آزمایش: اندازه گیری یون مس
وسایل آزمایش: بالن ژوژه- ترازو- ارلن مایر- بورت- پیپت حبابدار- پیپت فیلر
مواد آزمایش: پتاسیم یدات- پتاسیم یدید- محلول اسید سولفوریک- محلول چسب نشاسته- محلول تیوسولفات- پتاسیم تیوسیانات
تئوری آزمایش:
یدومتری
یون یدید یک عامل کاهنده ی نسبتاً موثری است که به طور وسیعی برای تجزیه ی اکسنده ها به کار می رود.
به طور کلی به واکنش هایی که در آن ید اکسید می گردد، یعنی ید از محلول یدیدها آزاد می گردد یدومتری گویند. روشهای زیادی بر اساس خواص کاهندگی یون یدید استوارند. ید که محصول واکنش است، معمولاً با محلول استاندارد تیوسولفات تیتر می شود.
عناصر زیادی را می توان به روش یدمتری تعیین نمود. یکی از این عناصر، مس است. در این روش از واکنش زیر جهت احیا و رسوب دادن مس استفاده می کنند.
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 2:1 منتشر شده است
نام آزمایش
تیتراسیون آهن (II) با سریم (IV)
عنوان
تیتراسیون آهن (II) با سریم (IV)
هدف
اندازه گیری درصد آهن در یک ترکیب از طریق تیتراسیون پتانسیومتری آهن (II ) با محلول استاندارد سریک آمونیوم نیترات
مواد لازم
تیتر شونده: آهن (II ) با غلظت 0.1 مولار
تیتر کننده: محلول 0.1 مولار سریک آمونیوم نیترات
وسايل لازم
مگنت ، بشر ، بالن ژوژه ، پیپت حبابدار ، بورت،پایه بورت،همزن مغناطیسی،الکترود شناساگر پلاتین،الکترود مرجع
تئوری :
به معناي سنجش و اندازه گيري پتانسيل است. در شاخه اي از شيمي به نام الكتروشيمي ، بحث از پيل الكتروشيميايي است. پيل الكتروشيميايي دستگاهي است كه انرژي واكنش شيميايي را كه در شرايط معمولي اغلب به صورت انرژي گرمايي آزاد مي شود، به انرژي الكتريكي قابل استفاده تبديل مي نمايد و مانند سدهاي هيدروالكتريك، مانع از به هدر رفتن انرژي مي شود. دو الكترود و يك پل نمكي ، تشكيل يك پيل را مي دهند. درواقع دو الكترود به دليل رقابت براي تبادل الكترون، تمايل متفاوت براي گرفتن الكترون دارند و اين تفاوت گرفتن الكترون، در شرايط مناسب سبب انتقال الكتريسيته مي شود. اين جريان الكتريسيته داراي يك ولتاژ يا پتانسيل خاص مي باشد كه با دستگاه ولت سنج قابل اندازه گيري است.
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 1:58 منتشر شده است
گزارشکار تعیین درصد خلوص مواد شیمیایی
نويسنده : کامران مومن زاده
تئوری آزمایش:
پیوندهای شیمیایی اسید سیتریک
اسید استیک یا جوهر انگور جز اسیدهای کربوکسیلیک است و در نامگذاری آیوپاک به اسید اتانوئیک معروف است.
نگاه کلی اسید استیک جز اسیدهای کربوکسیلیک میباشد و در نامگذاری آیوپاک به اسید اتانوئیک معروف است. این اسید دارای فرمول شیمیایی میباشد و در قسمت چشایی طعم ترشی ، شبیه طعم سرکه میدهد.
باکتریهای مخمر سرکه به دلیل تمایل به تولید اسید استیک به این نام معروف شدهاند. این باکتریها در مواد غذایی ، آب و خاک یافت میشوند. اسید استیک بطور طبیعی از میوهها و برخی مواد غذایی فاسد شده از فرایند تخمیر تولید میشوند و از قدیمیترین ترکیبات شیمیایی شناخته شده توسط انسان میباشد. تاریخچه سرکه (اسید استیک رقیق) از دوران باستان برای انسان شناخته شده بود. احتمالاً انسانها در دوران باستان هنگام تهیه شراب از فرایند تخمیر به وجود سرکه پی برده بودند. فیلسوف یونانی تئوفاراستوس در سه قرن پیش از میلاد چگونگی واکنش سرکه با فلزات و تولید رنگدانه برای استفاده در نقاشی از کربنات سرب و زاجهای سبز ایجاد شده از نمکهای مس و استات مس را توضیح دادهاست. رومیان باستان با نگهداری شراب ترش در قدحهای سربی ، شراب بسیار شیرینی به نام Sapa تولید میکردند که طعم شیرین آن ناشی از استات سرب بودهاست که امروزه دانشمندان مرگ زودرس بسیاری از اشراف روم را به مسمومیت ناشی از این ماده نسبت دادهاند. شیمیدانهای عصر رنسانس اسید استیک گلاسیال (منجمد) را از تقطیر خشک استاتهای فلزی تهیه میکردند. در سال ۱۸۴۷ هرمن کولب شیمیدان آلمانی برای اولین بار اسید استیک را از مواد معدنی سنتز کرد. خواص اسید استیک خالص، مایعی بیرنگ با بویی تیز، مایعی خورنده و قابل اشتعال میباشد. این اسید در ۱۶٫۶ درجه سانتیگراد منجمد میشود. به این دلیل و همچنین ظاهر یخ مانند آن به نام اسید استیک گلاسیال معروف است. اسید استیک در محلولهای آبی میتواند تفکیک شده و یون استات تولید کند. PH آن برابر با ۴٫۸ میباشد، یعنی در PH=۴٫۸ نیمی از مولکولهای اسید استیک در محلول آبی به صورت یون استات هستند. اسید استیک در حالت بخار شامل دیمرهایی از دو مولکول اسید استیک میباشد که با پیوند هیدروژنی با یکدیگر ارتباط دارند.
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 1:53 منتشر شده است
گزارش کار ازمایش اندازه گیری انرژی اکتیواسیون
عنوان : ازمایش اندازه گیری انرژی اکتیواسیون
هدف : اندازه گیری انرژی اکتیواسیون
تئوري آزمايش :
انرژي اكتيواسيون يكي از پارامترهاي در انجام واكنش هاي شيميايي است.
اثر دما بر ثابت سرعت واكنش به صورت زير خواهد بود :
اگر از طرفين رابطة فوق Ln بگيريم ، رابطه به صورت زير ساده مي شود
در دو دماي مختلف مقدار K به صورت زير خواهد بود :
از تفاضل دو رابطة بالا داريم
موضوع آزمايش: اندازه گيري انرژي اكتيواسيون
شرح آزمايش :
ابتدا محلول استات اتيل و محلول سود بسازيد.
از هر يك از اين محلول ها برداشته و به حجم برسانيد .
هدايت هر يك از اين محلول ها را به وسيلة كنداكتومتر اندازه بگيريد . (محلول سود را و محلول استات سديم را در نظر مي گيريم )
سپس از هر يك از اين محلول ها را برداشته و با هم مخلوط مي كنيم ، ميزان هدايت را در زمان هاي مختلف يادداشت مي كنيم .
اين آزمايش را در دو دماي انجام مي دهيم .
نتايج و محاسبات انجام شده :
1 7 6.74 -44.58
2 14 6.09 -10.86
3 21 5.56 -7.04
4 28 5.29 -6.05
5 35 5.03 -5.36
6 42 4.78 -4.85
1 7 8.69 -6.08
2 14 7.32 -3.89
3 21 6.69 -3.41
4 28 6.27 -3.17
5 35 5.71 -2.92
6 42 5.61 -2.88
این متن ناقص است برای مشاهده متن کامل آن را دانلود نمایید.
در صورت خراب بودن لینک دانلود " در قسمت نظر دهید " به ما اطلاع دهید تا مشکل را رفع کنیم
حجم فایل : 50 کیلو بایت | فرمت فایل : Docx | زبان : فارسی
دانلود مستقیم | پسورد فایل : kimiagari.ir
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 1:49 منتشر شده است
گزارش کار تبلور مجدد
استاد :سحر ملکي
نويسنده : کامران مومن زاده
تبلور مجدد
تبلور مجدد یکی از بهترین روش های خالص سازی برای خالص کردن یک جامد است.در این روش اختلاف در حلالیت سبب جدا شدن اجسام از یک دیگر و یا سبب جدا شدن ناخالصی از یک جسم میشود.در تبلور مجدد مولکول ها به تدریج از محلول جدا شده و در ردیف های منظمی به یکدیگر متصل می گردند که به عنوان شبکه شناخته می شوند. در این روش ساختمان بلورین جسم جامد را با انحلال در حلال مناسب بطور کامل از بین می برند و سپس اجازه می دهند تا بلورهای جسم به صورت یک شبکه بلوری مجددا تشکیل شوند.نا خالصی ها معمولا در محلول باقی می مانند.
تبلور مجدد شامل چندین مرحله می باشد:
۱)انتخاب حلال مناسب
۲)انحلال جسم مورد تخلیص در نقطه جوش یا نزدیک آن
۳)صاف کردن محلول داغ برای جدا نمودن ناخالصی های نامحلول
۴)تبلور از محلولی که در حال سرد شدن است
۵)جدا کردن بلورها از محلولی که در آن شناور هستند
۶)شستشوی بلورها برای خارج کردن محلولی که به آنها آغشته است
۷)خشک کردن بلورها
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 1:47 منتشر شده است
گزارش کار اندازه گیری نقطه جوش
استاد :سحر ملکي
نويسنده : کامران مومن زاده
اندازه گیری نقطه جوش
تعریف نقطه جوش:نقطه جوش دمایی است که در آن دما, فشار بخار جسم مایع با فشار اتمسفر برابر می شود.
نقطه جوش به عوامل زیر بستگی دارد:
۱_ فشار: بین نقطه جوش وفشار ارتباط مستقیم وجود دارد . اگر به تعریف نقطه جوش دقت شود فشار سیستم بالا رود نقطه جوش نیز بالا می رود و بالعکس.
تاثیر فشار بر نقطه جوش:
نقطه جوش یک مایع با تغییر فشار خارجی تغییر میکند. نقطه جوش نرمال یک مایع ، دمایی است که در آن فشار بخار مایع برابر با یک اتمسفر باشد . نقطه جوش داده شده در کتابهای مرجع ، نقاط جوش نرمال میباشند . نقطه جوش یک مایع را میتوان از منحنی فشار بخار آن بدست آورد و آن دمایی است که در آن فشار بخار مایع با فشار وارد بر سطح آن برابری میکند.
نوسانات فشار جو در یک موقعیت جغرافیایی ، نقطه جوش آب را حداکثر تا Cْ ۲ تغییر میدهد . ولی تغییر محل ممکن است باعث تغییرات بیشتر شود ، متوسط فشاری که هواسنج در سطح دریا نشان میدهد یک اتمسفر ، ولی در ارتفاعات بالاتر کمتر از این مقدار است. مثلا در ارتفاع ۵۰۰۰ پایی از سطح دریا متوسط فشاری که فشارسنج نشان میدهد atm 0.836 است و نقطه جوش آب در این فشار Cْ ۹۵٫۱ میباشد.
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 1:45 منتشر شده است
گزارش کار سنتز بنزوئیک اسید از تولوئن

بنزوئیک اسید، (C7H6O2 (C6H5COOH، یک ترکیب بلوری بی رنگ (سفید دیده میشود) است. بنزوئیک اسید سادهترین کربوکسیلیک اسید آروماتیک نیز میباشد. این ماده یک اسید ضعیف محسوب میشود. از نمکهای آن به عنوان نگهدارندههای غذایی استفاده میشود، همچنین در ساخت بسیاری از ترکیبات آلی دیگر از بنزوئیک اسید استفاده میشود.
تاریخچه
بنزوئیک اسید در قرن شانزدهم میلادی کشف شد. اولین بار شخصی به نام Nostradamus از تقطیر خشک مادهای سنتی به نام gum benzoin بدست آورد. در سال ۱۸۷۵ شخصی به نام Salkowski نیز پی به خواص ضد قارچ بنزوئیک اسید برد.
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 1:42 منتشر شده است
عنوان آزمایش: تهیه اتیلن
(برای تهیه ی اتیلن روش کارهای مختلفی را می توان در کتابهای شیمی و اینترنت پیدا کرد.اما با وجود یکسان بودن اصل روش،گاهاً دستور کار چندان ساده و ملموس نیست.در این مطلب سعی می کنم ساده ترین روش تهیه اتیلن را که در هر آزمایشگاه شیمی و با ساده ترین امکانات قابل انجام است،بنویسم.)
هدف: تهیه ی اتیلن به روش آزمایشگاهی از اتانول و شناسایی آن با محلول پتاسیم پرمنگنات
مقدمه:
اتیلن ساده ترین آلکن با فرمول C2H4 است.که گازی است بی رنگ و بسیار آتش گیر.
برای تهیه اتیلن روش های مختلفی وجود دارد که از جمله می توان کراکینگ گرمایی اتان(1) و آبگیری از الکل(اتانول) (2)را نام برد.که روش اول صنعتی و روش دوم بیشتر جنبه ی آزمایشگاهی دارد.
(1) CH3-CH3 => CH2=CH2 + H2
(2) CH3-CH2-OH => CH2=CH2 + H2O
اتیلن ( و سایر آلکن ها) با پتاسیم پرمنگنات اکسید می شوند و به این ترتیب رنگ ارغوانی آن را تغییر می دهند.همچنین با آب برم نیز واکنش داده و رنگ قرمز قهوه ای آن را از بین می برند.(روش های شناسایی آلکن ها)
(C2H4 + 2KMnO4+4H2O= 3 C2H4(OH)2 + 2KOH + 2MnO2(s
MnO2 منگنز دی اکسید (قهوه ای رنگ)
KMnO4 پتاسیم پرمنگنات (ارغوانی)
پس تغییر رنگ در طی شناسایی از ارغوانی به قهوه ای خواهد بود.
در صورت استفاده از آب برم تغییر رنگ از قهوه ای یا زرد آب برم به بی رنگ خواهد بود.
C2H4+Br2= C2H4Br2
Br2: برم( قهوه ای یا زرد رنگ)
C2H4Br2 : دی برمو اتیلن (بی رنگ)
در انتها می توان گاز خروجی از لوله ازمایش را با احتیاط آتش زد،که در این صورت گاز اتیلن شعله ور می شود.
از اتیلن در صنعت برای تهیه پلاستیک پلی اتیلن بسیار استفاده می شود.همچنین اتیلن نوعی هورمون گیاهی است که در کشاورزی برای رسیدن میوه هایی که بصورت نارس چیده می شوند(مثل موز) استفاده می شود.
روش کار:
یک تکه پنبه کوچک را به کمک همزن شیشه ای یا یک پیپت در ته یک لوله آزمایش بزرگ قرار می دهیم.چند سی سی اتانول را توسط پیپت روی پنبه ای که ته لوله آزمایش گذاشته ایم،میریزیم،به طوری که کاملاً آغشته به الکل شود.(این آغشته شدن به الکل باید در حدی باشد که موقع افقی کردن لوله آزمایش الکل از پنبه نریزد.) سپس لوله آزمایش را به صورت افقی به میله و پایه ی فلزی وصل می کنیم.به کمک اسپاتول مقداری پودر آلومینیوم اکسید(آلومین) را در وسط لوله آزمایش قرار می دهیم.در لوله آزمایش را با یک درپوش سوراخ دار بسته و لوله ی شیشه ای خمیده ای را به آن وصل می کنیم.(مطابق شکل).
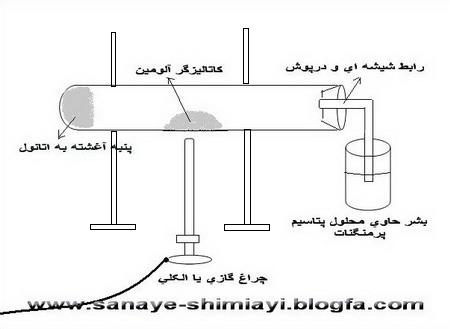
در یک بشر کوچک 50 سی سی تا نصف بشر محلول رقیق پتاسیم پرمنگنات( حدود 0.3% ) می ریزیم.و آن را زیر لوله رابط متصل به لوله آزمایش قرار می دهیم.حرارت را(در زیر قسمتی که آلومین قرار داده ایم) آغاز می کنیم.(گاهی نیز شعله را به سمت ته لوله آزمایش(جایی که پنبه را قرار داده ایم می بریم).اتانول در اثر حرارت و به کمک کاتالیزگر،آب زدایی شده و اتیلن تولید می کند.خروج گاز از لوله ی آزمایش با ایجاد حباب در محلول داخل بشر ثابت می شود.بخشی از این گاز بخار آب است و بخشی از آن گاز اتیلن.
با ورود اتیلن به داخل محلول پتاسیم پرمنگنات رنگ آن قهوه ای یا بی رنگ می شود.( بسته به اینکه محیط اسیدی باشد یا نه).
درست به همین روش می توان به جای پتاسیم پرمنگنات از آب برم نیز برای شناسایی اتیلن استفاده کرد.(بهتر است به جای برم از همن محلول پتاسی پرمنگنات برای ناسایی استفاده کرد چون برم سمی است و باعث سوختگی شدید پوست می شود)
در پایان گزارشکار باید نتیجه ی آزمایش و منابع احتمالی خطا را ذکر کرده و با توجه به مطالب گفته شده در مقدمه و متن روش کار،می توان به سوالات مربوطه پاسخ داد.
زندگینامه ی مندلیف

دیمتری ایوانویچ مندلیف شیمیدان بزرگ روسی در فوریه 1834 در شهر «توبوسك» در سیبری روسیه متولد شد او چهاردهمین فرزند خانواده بود پدرش مدیر مدرسه بود او پدر خود را در کودکی از دست داد. او در مدرسه توپولسک استعداد درخشان خود را در ریاضی و فیزیک نشان داد و عصرها بعد مدرسه در کارگاه شیشه گری به مادرش کمک می کرد مدتی بعد کارگاه شیشه گری آتش گرفت و همه سرمایه شان از دست رفت. دیمیتری برای یافتن شغل بهتر به سن پترزبورگ رفت و در آن جا به تدریس پرداخت در سال 1850 توانست بورس تحصیلی بگیرد و به تحصیل در رشته ریاضی، فیزیک و شیمی بپردازد. او خانواده خود را هم به سن پترزبورگ برد اما متاسفانه مادر و خواهرش به بیماری سل دچار شدند و جان خود را از دست دادند و او تنها شد فقر از یک سو و اندوه از سوی دیگر او را چنان بیمار ساخت که پزشکان تصور کردند او نیز به سل میتلا شده است و به او توصیه نمودند برای معالجه و استراحت به یک محل خوش آب و هوا مسافرت نماید. دیمیتری به جزایر کریمه رفت و مدتی را در آنجا ماند. پس از مدتی او سلامت روحی خود را بازیافت و به سنت پترزبورگ بازگشت...
عنوان آزمایش: خالص سازی مواد به روش استخراج
هدف: استخراج آدیپیک اسید از فاز آبی به فاز آلی(اتر)
تئوری آزمایش:
استخراج روشی است برای جداسازی که در آن جسمی از یک فاز به فاز دیگر منتقل می شود. در بعضی مواقع لازم است برای بازیابی یک ماده آلی از راههایی غیر از تقطیر استفاده شود. یکی از این راهها تماس دادن محلول آبی با یک حلال غیر قابل اختلاط با آب است. اگر حلال مناسب باشد، بیشتر مواد آلی(در اینجا آدیپیک اسید) از لایه آبی به حلال آلی (که با آب امتزاج ناپذیر است) انتقال پیدا میکند.
از نظر کمی پخش یک جسم بین دو حلال غیر قابل امتزاج را بر حسب ضریب پخش K بیان میکنند. به عبارت دیگر ضریب پخش(k) یعنی: نسبت غلظت ماده ی حل شده در حلال اول، به غلظت همان ماده در حلال دوم.
حلالی که برای استخراج انتخاب می شود باید دارای این ویژگیها باشد:
1- با حلالی که دارای ماده مورد نظر است،مخلوط نشود.(سیستم دو فازی تشکیل دهد)
2- K ماده در حلال انتخاب شده بزرگ باشد. (یعنی ماده در حلال دوم بیشتر از حلال اول محلول باشد)
3- حلال نباید ما ماده مورد نظر واکنش دهد.
4- حلال انتخاب شده به آسانی تبخیر شود.
5- حلال نباید ناخالصی ها را استخراج کند.
در استخراج مایع-مایع از قیف جدا کننده (دکانتور) استفاده می شود.قیف نباید بیشتر از سه چهارم حجم آن پر شود چون در این صورت امکان هم زدن محلول وجود نخواهد داشت.هدف از تکان دادن و هم زدن این است که سطح تماس دو حلال افزایش یابد و ماده حل شده در حلال اول در مدت زمان کمتری بتواند به حلال دوم برود.(در آن حل شود).هر چند ثانیه یک بار باید قیف را برگرداند(شیر به سمت بالا) و آن را به آرامی باز کرد تا گاز قیف خارج شود.این عمل همیشه باید انجام شود ولی در دو حالت اهمیت بیشتری دارد:
1- وقتی که حلال مورد استفاده دمای جوش پایینی داشته باشد.
2- یک محلول اسیدی با محلولی از سدیم بیکربنات استخراج شود.(در این حالت گاز کربن دی اکسید آزاد می شود)
NaHCO3 + HA = NaA + H2O + CO2
پس از تکان دادن قیف و خارج کردن گازهای آن، قیف جدا کننده را روی گیره ی حلقه ای قرار می دهند و فرصت می دهند تا فازها به خوبی از هم جدا شوند.
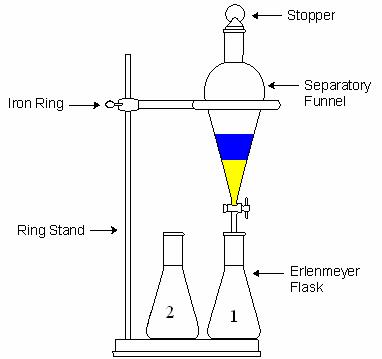
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 1:38 منتشر شده است
گزارش کار انرژی آزاد گیبس
انرژی آزاد گیبس را میتوان از این معادلات بدست آورد:
این فرمولها دربرگیرندهٔ دو عامل است که در انجامپذیری واکنشها در طبیعت مؤثرند: آنتالپی (انرژی سیستم) و آنتروپی (بینظمی سیستم).
انتالپی (H) تغییرات انرژی ضمن انجام واکنش را دربرمیگیرد. این تغییرات هم انرژی جنبشی راشامل میشود و هم انرژی پتانسیل را، به شرط آن که در حین انجام واکنش فشار وارد بر سیستم ثابت باشد.
یک واکنش زمانی از نظر انرژی انجامپذیر تلقی میشود که بر اثر انجام آن انرژی سیستم کمتر شود. به عبارت بهتر سیستم پایدارتر شود. در این صورت تغییرات انتالپی منفی خواهد بود.
اما در اطراف ما بسیاری از واکنشها اتفاق میافتند که در آنها سیستم گرما میگیرد و انرژی آن افزایش مییابد، یعنی تغییرات انتالپی در آنها مثبت است. این گونه واکنشها به علت عامل دوم رخ میدهند که آنتروپی نامیده میشود و با S نشان داده میشود. این عامل نشاندهندهٔ میزان بینظمی سیستم است و زمانی مساعد است که انجام واکنش سبب زیادشدن بینظمی در سیستم شود. در فرمول انرژی آزاد گیبس عامل S در T ضرب میشود که دمای مطلق (کلوین) گاز است، یعنی اثر عامل بینظمی در دمای بالا بیشتر است.
وجود نقص موجب افزایش در آنتروپی شبکه میشود و بنابراین همه جامدات تمایل به وجود نقص دارند. G = H - TS
افزایشS ، یک جمله منفی در انرژی آزاد وارد میکند. اگر ایجاد نقص گرماگیر باشد،H مثبت میشود ولی ، بزرگتر از صفر خواهد بود و باز هم انرژی آزاد منفیمیشود. با افزایش دما ، نقصها افزایش مییابد و G منفی تر میشود.
قانون اول ترمودینامیک
قانون اول ترمودینامیک به معرفی انرژی درونی ، U ، منجر شد. این کمیت تابع حالتیاست که بر مبنای آن ، مجاز بودن یک فرآیند مورد قضاوت قرار میگیرد وبیان میدارد که فقط تحولاتی مجاز است که انرژی داخلی کل سیستم منزوی ،ثابت بماند. قانونی که ملاک خودبخودی بودن را مشخص میسازد (قانون دوم ترمودینامیک) ، برحسب تابع حالت دیگری بیان میشود. این تابع حالت ،آنتروپی ، S ، است.
ملاحظه خواهیم کرد که بر مبنای آنتروپی قضاوتمیکنیم که آیا یک حالت بطور خودبخودی از حالت دیگری قابل حصول میباشد.در قانون اول با استفاده از انرژی داخلی ، تحولات مجاز مشخص میشود(آنهایی که انرژی ثابت دارند). از قانون دوم با استفاده از آنتروپی ،تحولات خودبخودی از بین همان فرآیندهایی مشخص میشود که بر مبنای قانوناول مجاز میباشد.
بیان قانون دوم
آنتروپی سیستم منزوی در یک فرآیند خودبخودی افزایش مییابد:
که ، آنتروپی تمام قسمتهای سیستم منزوی میباشد.
ازآنجایی که فرآیندهای برگشت ناپذیر (مانند سرد شدن شیئی تا دمای محیط وانبساط آزاد گازها) خودبخودی است، در نتیجه همه آنها با افزایش آنتروپیتوام میباشند. این نکته را میتوان به این صورت مطرح کرد که در فرایندهایبرگشت ناپذیر آنتروپی تولید میشود. از طرف دیگر ، در فرایند برگشت پذیرتوازن وجود دارد، یعنی سیستم با محیط در هر مرحله در تعادل است. هر مرحلهبسیار کوچک در این مسیر برگشت پذیر بوده و پخش نامنظم انرژی روی نمیدهد ودر نتیجه آنتروپی افزایش نمییابد، یعنی در فرآیند برگشت پذیر آنتروپیایجاد نمیشود. آنتروپی در فرآیندهای برگشت پذیر از بخشی از سیستم منزویبه بخش دیگری منتقل میگردد.
تعریف آماری آنتروپی
بر مبنای تعریفآماری ، فرض میشود که در واقع میتوانیم با استفاده از فرمول ارائه شدهتوسط لوودیگ بولتزمن (Ludwing Boltzmann) در سال 1896 ، آنتروپی را محاسبهکنیم:
که k، ثابت بولتزمن است:
این ثابت به صورت به ثابت گازربط دارد. کمیت W تعداد راههای متفاوتی است که سیستم میتواند با توزیعاتمها یا مولکولها بر روی حالتهای در دسترس به انرژی خاصی برسد. واحدآنتروپی با واحد k یکسان است. در نتیجه واحد آنتروپی مولی ، میباشد؛ (اینبا واحد R و ظرفیت گرمایی یکی است.)
تعریف ترمودینامیکی انرژی
درروش ترمودینامیکی ، تمرکز بر روی تغییر آنتروپی در طول یک فرایند ، dS ،میباشد، نه مقدار معلق S. تعریف dS بر این مبناست که میتوان میزان پخشانرژی را به انرژی مبادله شده به صورت گرما ، در حین انجام فرایند ربطداد. تعاریف آماری و ترمودینامیکی با هم سازگار میباشند. در شیمی فیزیکاین یک لحظه نشاط آور است که بین خواص تودهای (که مورد نظر ترمودینامیکاست) و خواص اتمها یک ارتباط برقرار شود.
تغییر آنتروپی محیط
تغییرآنتروپی محیط را با علامت 'dS نشان میدهیم. علامت پریم مربوط به محیطسیستم واقعی که در سیستم منزوی بزرگ قرار دارد، مربوط میشود. محیط را بایک مخزن حرارتی بزرگ (عملا یک حمام آب) نشان میدهیم که در دمای T باقیمیماند. مقدار گرمای منتقل شده به مخزن در اثر انجام کار مانند سقوط یکوزنه را با 'dq نشان میدهیم که این گرما به مخزن منتقل میشود. هرچهمقدار گرمای بیشتری به مخزن منتقل شود، حرکت حرارتی بیشتری هم در آن ایجادمیشود و از این رو ، پخش انرژی به میزان بیشتری اتفاق میافتد. از ایننکته استنباط میشود که:
اگر گرما به مخزن سردی منتقل شود،کیفیت انرژی نسبت به موردی که آن گرما به مخزن گرمتری داده شود، انحطاطبیشتری خواهد داشت. در مورد اخیر میتوانیم در اثر جاری شدن گرمای 'dq ازیک مخزن سرد به مخزن سردتری کار استخراج کنیم، اما اگر این گرما مستقما بهمخزن سردتر منتقل شود، استخراج چنین کاری امکان پذیر نیست.
نتیجه میگیریم که اگر مقدار معین انرژی به صورت گرما به مخزن گرمی داده شود،آنتروپی کمتری ایجاد میشود تا اینکه آن انرژی به مخزن سردی داده شود.سادهترین راهی که میتوان این وابستگی دمایی را به حساب آورد، چنین است:
که 'T دمایی است که در آن دما ، انتقال گرما صورت گرفته است. برای یک تغییر قابل اندازه گیری در دمای ثابت چنین داریم:
وقتی که مقدار زیادی حرکت حرارتی در دمای پایین ایجاد شود، تغییر آنتروپی بزرگی اتفاق میافتد. برای فرآیند آدیاباتیک:
0 = 'q وقتی 0 = 'S∆
این نتیجه برای هر فرآیندی ، برگشت پذیر یا برگشت ناپذیر ، صحیح است، تا زمانیکه مناطق گرم محلی در محیط ایجاد نشود، یعنی زمانی این نتیجه صحیح است کهمحیط ، تعادل درونی خود را حفظ کند. اگر مناطقی محلی بوجود آید، انرژی ازاین مناطق بطور خودبخودی پخش میشود و در نتیجه آن آنتروپی تولید میشود.موقعی که یک واکنش شیمیایی با تغییر آنتالپی H∆ در سیستمی انجام میشود،گرمایی که در فشار ثابت وارد محیط میشود،
برابر با . بنابراین تغییر آنتروپی محیط برابر است با:
انرژیداخلی V و آنتروپی S ، دو تابع اساسی ، برای توصیف سیستمهای ترمودینامیکیدر حالت تعادلاند، هر سیستم ماکروسکوپیکی که متشکل از انبوه اتم ومولکولهاست، از قانون بقای انرژی تبعیت میکند. حرکت بزرگ مقیاس سیستم ازقانون بقای انرژی مکانیکی تبعیت میکند و در غیاب میدانهای الکترومغناطیسی، انرژی باقی مانده در سیستمی که منزوی است پایسته میماند، این کمیت همانانرژی داخلی است.
قانون دوم
اين برای شما نوشته شده استبرای اينکه قانون دوم ترموديناميک و انتروپی را به سادگی درک کنيد.همه بهجز تعدادی از متون شيمی که به طور کلی نوشته می شوند بيان می کنند کهانتروپی يعنی بی نظمی.به هر حال اگر متن يا آموزگار شما چيزها را به طرزیمتفاوت توصيف می کند بحث نکنيد که درست است يا غلط فقط به خاطر بسپاريد کهشما در متن چه می خوانيد و يا اينکه در کلاس چه می شنويد تا بتوانيد بهامتحان جواب درست بدهيد.امروزه نمرات در زندگی مهم هستند.( اما درک آنچهاين جا فرا می گيريد مدت زندگی را طولانی خواهد کرد.)
قانون دوم ترموديناميک
بسياریاز متون قانون دوم را اين گونه تعريف می کنند:انتروپی جهان در طی يکفرآيند خود به خودی افزايش می يابد؟و سپس qrev/T يا انرژی آزاد =ΔG و ΔSرا به شما می فهمانند.
فهم اين خيلی پيچيده است.هنگامی که سال اول مهندسی شيمی هستيم اين را خيلی ساده فرض می کنيم.
قانوندوم بر مبنای تجربه ی بشری است و از تئوری ها و معادلات پيچيده به دستنيامده است.بنابراين فکر کنيد در مورد تجربه ای که شما داشته ايد:يک سنگخواهد افتاد هنگامی که شما آن را بلند می کنيد و رها می کنيد.ماهی تابه ومواد داخل آن سرد خواهد شد هنگامی که آن را از روی چراغ گاز بر میداريد.آهن در هوا زنگ می زند.هوا در لاستيک های با فشار بالا از يک سوراخکوچک به شدت خارج می شود تا به فشار پايين اتمسفری برسد.تکه های يخ در يکاتاق گرم ذوب می شوند.
در اين فرآيند ها چه اتفاقی می افتد؟بعضی ازانواع انرژی از متمرکز شدن ( متمرکز شدن در سنگ يا ماهی تابه و ...) بهپخش شدن تغيير می يابند.دوباره به مثال ها توجه کنيد تا اين تغيير را درهمه آن ها مشاهده کنيد.
خب اين هم يک راه ساده برای نشان دادن علم نهفته در قانون دوم:
انرژی به طور خود به خودی پخش می شود تا متمرکز نماند البته اگر عاملی آن را به تاخير نياندازد.
اماانتروپی و جهان چطور که در بسياری از متون هستند؟ به طور خلاصه انتروپی رااز نظر می گذرانيم ولی «جهان» فقط به معنی «سيستمی است که شما آن را بههمراه محيط اطرافش می بينيد يعنی هر چيزی که اطراف آن بسته است».سيستمبعلاوه محيط اطراف.اگر «سيستم بعلاوه محيط اطراف» شما را گيج می کند يااينکه شما دوست داريد جزئيات بيشتری در مورد سه فرآيند ذکر شده در بالابدانيد پاراگراف زير را بخوانيد.
۱.سنگ دارای انرژی پتانسيل است هنگامیکه شما آن را از سطح زمين بلند می کنيد.هنگامی که آن را رها می کنيد انرژیپتانسيل به جنبشی تبديل می شود همچنين هنگامی که سقوط می کند مولکول هایهوا را کنار می زند ( بنا براين مقداری از انرزی سنگ پراکنده می شود.)قبلاز اينکه که به زمين برخورد کند به مقدار ناچيزی انرژی صوت ( هوای فشرده )را پراکنده می کند و اندکی باعث گرم شدن خود و زمينی که به آن برخورد میکند می شود.سنگ بدون تغيير است ( پس از يک دقيقه که مقدار ناچيزی از گرمایبرخورد را در هوا پراکنده کرده است).ولی انرژی پتانسيلی که ماهيچه های شماصرف بالا بردن سنگ نمود اکنون در محيط اطراف پخش شده است کمی در حرکتمولکول های هوا و کمی گرم شدن زمين و هوا.{سيستم : سنگ بالای زمين و سپسروی زمين. محيط اطراف : هوا به همراه زمين .}
۲.اتم های آهن در ماهیتابه داغ به سرعت در حال ارتعاش هستند.بنابراين انرژی حرکتی در ماهی تابه داغ متمرکز است.انرژی حرکتی اگر بتواند پخش می شود.هر گاه مولکول های ( باحرکت کند تر )هوای سردتر اتاق به ماهی تابه داغ برخورد می کنند اتم های بهشدت مرتعش آهن مقداری از انرژی خود را به مولکول های هوا منتقل میکنند.بنابراين انرژی متمرکز ماهی تابه پخش می شود و به طور وسيع تر بينمولکول های هوا تقسيم می شود.
{ سيستم : ماهی تابه و محيط اطراف : هوای اتاق .}
۳.آهندر سوزن ها يا چيزهای ديگر نبايد داغ باشد ( يعنی حرکت بسيار شديد مولکولها يا اتم ها) برای اينکه انرژی متمرکز درون آن به صورت شميايی موجود باشد: اتم های آهن وبه همراه مولکول های اکسيژن موجود در هوا شامل يک انرژیشيميايی در ميان پيوندهای شيميايی خود هستند که اين انرژی از انرژی موجوددر زنگ آهن ( اکسيد آهن ) بيشتر است. (اين دليل واکنش اکسيژن با آهناست-آزاد کردن انرژی از سطح انرژی بالاتر موجود در پيوندهای اکسيژن بههمراه پيوندهای آهن و شکل دادن سطح انرژی پايين تر موجود در پيوند هایاکسيد آهن٫ با همه اين اختلاف در انرژی پخش شدن در محيط اطراف به صورتگرما نيز داريم يعنی واکنش گرمازا است و مولکول های محيط را وادار می کندکه سريع تر حرکت کنند.اما فراموش نکنيد که حتی موادی که مقدار زيادی انرژیدر پيوند های خود دارند از اين که اين انرژی را به صورت ناگهانی در محيطپخش کنند جلوگيری می شوند.مقدار زيادی انرژی لازم است برای اين که پيوندهای آن ها شکسته شود قبل يا در حين واکنش.با وجود اين که انرژی خيلیبيشتری ممکن است در نتيجه واکنش و تشکيل پيوند های جديد آزادشود.)بنابراين حتی در هوای مرطوب که سرعت فرآيند افزايش می يابد آهن بهطور خود به خودی ( ولی نه خيلی سريع ) با اکسيژن واکنش می دهد و هر کدامانرژی های موجود در پيوند های خود را در محيط پخش می کنند هنگامی که آهنبا اکسيژن اکسید آهن را تشکيل می دهند.{سيستم : آهن٫اکسيژن و اکسيدآهن.محيط اطراف : هوای نزديک ٫ رطوبت يا نمک به همراه هر چيزی که با زنگآهن در تماس است.}
انتروپی چيست؟
انتروپی پخش شدن خود به خودی انرژیرا نشان می دهد: چه مقدار انرژی در يک فرآيند پخش می شود٫يا با چه وسعتیپخش می شود-در يک دمای خاص.(بعضی وقت ها يک معادله ساده٫تغييراتانتروپی=دما/انرژی پخش شده يا qreversible/T و هنگام تغيير فاز مانند ذوبو تبخير عبارت است از ΔS = ΔHfusion /T or ΔHvaporization /T .)
در شيمی انرژی که انتروپی را بيان می کند عبارت است از «انرژی حرکتي» ٫ انرژی انتقالی٫ارتعاشی و چرخشی مولکول ها
وΔH انرژی تغيير فاز -در بسياری از معادلات هم انرژی حرکتی و هم انرژیتغيير فاز با "q" يا ΔH نشان داده می شوند.«انرژی پيوند» انرژی پتانسيل کهبا پيوند های شيميايی در ارتباط است و ما در مثال اکسيد شدن آهن در موردآن صحبت کرديم٫ فقط به وسيله انرژی پتانسيل تشکيل پيوند ها اندازه گيری میشود.در اين مورد نيز در مثال مذکور اندکی بحث شد.و اين نيز فقط به وسيلهتغيير انتروپی هنگام انجام واکنش با رابطه ΔG = ΔH - T ΔS اندازه گيری میشود.
آيا اين توصيف از تغيير انتروپی پيچيده است؟انتروپی يک نوع مقياس«قبل و بعد» فلسفی و علمی است-اندازه گيری مقدار انرژی منتشر شده تقسيم بردما يا وسعت پخش شدگی انرژی پس از اينکه چيزی اتفاق می افتد ( در يک دمایثابت).هنگامی که اولين رابطه مربوط به انتروپی در يک فرآيند برگشت پذيرديده می شود ابتدا ممکن است گيج کننده و خلاصه به نظر برسد.اجازه دهيد بهآن با استفاده از عبارت «چه مقدار» بنگريم٫يک مثال عملی: يخ در اتاق گرمبه طور خود به خودی ذوب می شود.(تغيير فاز و افزايش انتروپی ).
تغيير فاز -«چه مقدار» انرژی در اين مثال پخش شده است.
ازتجربه خود -به ياد آوريد که اين مبنا و اساس قانون دوم است-شما فکر میکنيد انرژی مولکول ها در چه جهتی حرکت کرده است.از آن مولکول های سريعموجود در هوای اتاق به سمت مولکول های کند يخ يا اينکه مولکول های کند تريخ انرژی خود را به هوای گرم داده اند.مطمئناً هميشه از گرم تر بهسردتر.انرژی حرکتی بيشتر مولکول های هوا مقداری انرژی را در يخ سرد پخشکرده اند و پيوند های هيدروژنی بين مولکول های آب در يخ را شکسته يادگرگون ساخته اند.آب مايع در کوچک ترين دمای بالای نقطه ذوب شکل می گيرد وبالعکس يخ جامد در کوچک ترين دمای زير نقطه ذوب به وجود می آيد.
هنگامیکه مولکول های گرمتر هوا مقداری از انرژی حرکتی خود را منتقل می کنند تادر يخ پخش شود٫ بسياری از پيوند های هيدروژنی در يخ شکسته می شود.اين بهمولکول ها اجازه می دهد که با همان مقدار انرژی که در اثر ارتعاش در يخدارا بودند حرکت کنند اما اکنون پيوند های جديدی با مولکول های ديگر آبمايع شکل گرفته است ٫و در واقع حرکت کمی دارند اما در مقايسه با حالت جامدبسيار زياد است.(سرعت آن ها افزايش نمی يابد٫ و به اين ترتيب مجموع انرژیجنبشی مايع بدون تغيير است و هنگامی که يخ ذوب می شود دما از ۲۷۳ کلوينبالاتر نمی رود.)به هر حال اين فقط يک افزايش در انرژی پتانسيل آب مايع در۲۷۳ کلوين در مقايسه با يخ است٫ ديگر همه مولکول ها در چهارچوب بسيار محکميخ گرفتار نيستند.آن ها هنوز پيوندهای هيدروژنی در آب هستند اما با شکلدادن پيوندهای جديد و شکستن پيوند های ديگر به طور ثابت در مايع حرکت میکنند.
با شکستن آن پيوند های هيدروژنی اوليه و اجازه دادن به مولکول هابرای اينکه آزادانه حرکت کنند چه مقدار انرژی در ذوب يخ پخش می شود؟ البتهبه اندازه آنتالپی ذوب يخ! به اين دليل است که متن شما افزايش انتروپی رادر ذوب يخ ΔS = qrev /T = ΔH/T بيان می کند.
انتروپی استانداردـ «چه مقدار» انرژی يک نمونه پخش شده است.
بسياریاز متون از انتروپی استاندارد (So298) همه عناصر و ترکيبات سخن میگويند.در واقع ٫ انتروپی استاندارد بايد «تغيير انتروپی استاندارد» برایمواد ناميده می شد.اين به اين خاطر است که مقدار So298 که در جداول ليستمی شود در واقع مجموع انرژی(qrev ) است که به طور برگشت پذير پخش شده است( در هر نسبت افزايشی از دما يعنی qrev/T )
این مطلب در تاریخ: دو شنبه 25 آذر 1392 ساعت: 1:29 منتشر شده است
تقطیر و انواع آن
استاد : خانم سحر ملکی
نویسنده : کامران مومن زاده
روشهای مختلفی برای جداسازی مواد اجزای سازنده یک محلول وجود دارد که یکی از این روشها فرایند تقطیر میباشد در روش تقطیر جداکردن اجزاء یک مخلوط ، از روی اختلاف نقطه جوش آنها انجام میگیرد. تقطیر در عمل به دو روش زیر انجام میگیرد. روش اول شامل تولید بخار از طریق جوشاندن یک مخلوط مایع ، سپس میعان بخار ، بدون اینکه هیچ مایعی مجددا به محفظه تقطیر بازگردد. در نتیجه هیچ مایع برگشتی وجود ندارد. در روش دوم قسمتی از بخار مایع شده به دستگاه تقطیر باز میگردد و به صورتی که این مایع برگشتی در مجاورت بخاری که به طرف مبرد میرود قرار میگیرد. هر کدام از این روشها میتوانند پیوسته یا ناپیوسته باشند.
انواع تقطیر
- تقطیر ساده غیر مداوم : در این روش تقطیر ، مخلوط حرارت داده میشود تا بحال جوش درآید بخارهایی که تشکیل میشود غنی از جزء سبک مخلوط میباشد پس از عبور از کندانسورها (میعان کننده ها) تبدیل به مایع شده ، از سیستم تقطیر خارج میگردد. به تدریج که غلظت جزء سنگین مخلوط در مایع باقی مانده زیاد میشود، نقطه جوش آن بتدریج بالا میرود. به این ترتیب ، هر لحظه از عمل تقطیر ، ترکیب فاز بخار حاصل و مایع باقی مانده تغییر میکند.
- تقطیر ساده مداوم : در این روش ، مخلوط اولیه (خوراک دستگاه) بطور مداوم با مقدار ثابت در واحد زمان ، در گرم کننده گرم میشود تا مقداری از آن بصورت بخار درآید، و به محض ورود در ستون تقطیر ، جزء سبک مخلوط بخار از جزء سنگین جدا می شود و از بالای ستون تقطیر خارج میگردد و بعد از عبور از کندانسورها ، به صورت مایع در میآید جزء سنگین نیز از ته ستون تقطیر خارج میشود. قابل ذکر است که همیشه جزء سبک مقداری جزء سنگین و جزء سنگین نیز دارای مقداری از جزء سبک است.
- تقطیر تبخیر آنی (ناگهانی) : وقتی محلول چند جزئی مانند نفت خام را حرارت میدهیم، اجزای تشکیل دهنده آن بترتیب که سبکتر هستند، زودتر بخار میشود. برعکس وقتی بخواهیم این بخارها را سرد و دوباره تبدیل به مایع کنیم، هر کدام که سبکتر باشد دیرتر مایع میگردد. با توجه به این خاصیت ، میتوانیم نفت خام را به روش دیگری که به آن "تقطیر آنی" گویند، تقطیر نماییم. در این روش ، نفت خام را چنان حرارت میدهیم که ناگهان همه اجزای آن تبدیل به بخار گردد و سپس آنها را سرد میکنیم تا مایع شود. در اینجا ، بخارها به ترتیب سنگینی ، مایع میشوند یعنی هرچه سنگینتر باشند، زودتر مایع میگردند و بدین گونه ، اجزای نفت خام را با ترتیب مایع شدن از هم جدا میکنیم.
- تقطیر در خلا : با توجه به اینکه نقطه جوش مواد سنگین نفتی نسبتا بالاست و نیاز به دما و انرژی بیشتری دارد، و از طرف دیگر ، مقاومت این مواد در مقابل حرارت بالا کمتر میباشد و زودتر تجزیه میگردند، لذا برای جداکردن آنها از خلا نسبی استفاده میشود. در این صورت مواد دمای پایینتر از نقطه جوش معمولی خود به جوش میآیند. در نتیجه ، تقطیر در خلا ، دو فایده دارد: اول این که به انرژی و دمای کمتر نیاز است، دوم اینکه مولکولها تجزیه نمیشوند. امروزه در بیشتر موارد در عمل تقطیر ، از خلا استفاده میشود. یعنی این که: هم تقطیر جزء به جزء و هم تقطیر آنی را در خلا انجام میدهند.
- تقطیر به کمک بخار آب : یکی دیگر از طرق تقطیر آن است که بخار آب را در دستگاه تقطیر وارد میکنند در این صورت بی آنکه خلاءای ایجاد گردد، اجزای نفت خام در درجه حرارت کمتری تبخیر میشوند. این مورد معمولا در زمانی انجام میشود که در نقطه جوش آب ، فشار بخار اجزای جدا شونده بالا باشد تا به همراه بخار آب از مخلوط جدا گردند.
- تقطیر آزئوتروپی : از این روش تقطیر معمولا در مواردی که نقطه جوش اجزاء مخلوط بهم نزدیک باشند استفاده میشود، جداسازی مخلوط اولیه ، با افزایش یک حلال خاص که با یکی از اجزای کلیدی ، آزئوتوپ تشکیل میدهد امکانپذیر است. آزئوتروپ محصول تقطیر یا ته مانده را از ستون تشکیل میدهد و بعد حلال و جزء کلیدی را از هم جدا میکند. اغلب ، ماده افزوده شده آزئوتروپی با نقطه جوش پایین تشکیل میدهد که به آن شکننده آزئوتروپ میگویند. آزئوتروپ اغلب شامل اجزای خوراک است، اما نسبت اجزای کلیدی به سایر اجزای خوراک خیلی متفاوت بوده و بیشتر است.
این مطلب در تاریخ: یک شنبه 24 آذر 1392 ساعت: 6:52 منتشر شده است
دستور كار آزمايشگاه فيزيك پايه 2
دستور كار مقاومت الكتريكي با حرارت
دستور كار پديده هاي الكترومغناطيسي
دستور كار مقاومت الكتريكي با حرارت
دستور كار پديده هاي الكترومغناطيسي
این مطلب در تاریخ: یک شنبه 24 آذر 1392 ساعت: 6:47 منتشر شده است
برچسب ها : دستور كار آزمايشگاه فيزيك پايه 2,
سنتز استانیلید
استاد : خانم سحر ملکی
نویسنده :
کامران مومن زاده
عنوان:
سنتز استانیلید
هدف:
سنتز استانیلید از آنیلین و استیک انیدرید.
ابزار و مواد لازم:
پیست آب مقطر-ارلن-استوانه مدرج-پیپت-چراغ بونزن-ترازو-کاغذ صافی-قیف شیشه ای
آنیلین-استیک انیدرید-اسید سولفوریک
تئوری آزمایش:
آنیلین
انواع آنیلین
1) تجاری
2) خالص شیمیایی
کاربرد و مصارف
1) بطور وسیع در ساخت رنگهای نساجی و مواد میانی رنگهای نساجی استفاده می شود.
2) در صنایع لاستیک سازی ، از مشتقات آنیلین به عنوان تسریع کننده و تقویت و استحکام لاستیک و ضد اکسید شدن استفاده می شود.
3) در صنایع داروسازی ، آنیلین در ساخت داروهای سولفانیل آمید و عوامل شیرین کننده سنتتیک مصرف می شود.
4) آنیلین همچنین در صنایع انفجاری از اهمیت خاصی برخوردار است و در ساخت ژلاتین و نیتروتولوئن استفاده می شود.
این مطلب در تاریخ: یک شنبه 24 آذر 1392 ساعت: 6:35 منتشر شده است
دانلود گزارشکار آزمایشگاه فیزیک2 بالینک مستقیم و با فرمت ورد(word)


![]() فرمت: word
فرمت: word
![]() دانلود:دانلود فایل
دانلود:دانلود فایل
![]() رمز: oil-yasuj.vcp.ir
رمز: oil-yasuj.vcp.ir
این مطلب در تاریخ: یک شنبه 24 آذر 1392 ساعت: 6:26 منتشر شده است
هدف از انجام این آزمایش تهیه نمک مضاعف سولفات آمونیم مس(II) و نمک مضاعف سولفات آمونیم نیکل(II) و کمپلکس تترا آمین مس(II) و مقایسه پاره ای از خواص نمک ساده، نمک مضاعف و نمک کمپلکس و همچنین تهیه زاج های کروم، آلومینیوم و آهن با استفاده از واکنشگر های لازم و بررسی رشد بلوری آن ها می باشد.
در کمپلکس ها پیوند بین فلز و گروه های غیر فلزی دهنده الکترون (لیگاند) از نوع پیوند کئوردیناسیون می باشد. لیگاند ها را بسته به تعداد اتم کئوردینانس شونده، به لیگاند های یک دندانه، دو دندانه و... تقسیم می کنند. لیگاند های کی لیت دهنده می توانند همزمان از بیش از یک موقعیت به فلز متصل شوند. کی لیت ها کمپلکس هایی پایدارند و حلقه های 5 و 6 عضوی آن ها پایدارتر هستند.
Fe(CN)2 + 4 KCN → K2Fe(CN)6
AgCl + 2 NH3 → Ag(NH3)2Cl
پتاسیم هگزا سیانو فرات(II) در آب حل شده و محلولی را می دهد که هیچ نوع واکنش مشخص کننده یون Fe2+ ندارد، زیرا این یون در محیط آزاد نیست و به صورت [Fe(CN)6]4- وجود دارد. این یون یک یون کمپلکس است.
یک دسته معمول از نمک های مضاعف، زاج ها هستند که در حقیقت سولفات مضاعف پتاسیم و آلومینیم هستند.(KAl(SO4)2,12H2O)
این مطلب در تاریخ: یک شنبه 24 آذر 1392 ساعت: 5:54 منتشر شده است
برچسب ها : تهیه یک نمک مضاعف و یک کمپلکس و مقایسه آنها و تهیه زاجها و بررسی رشد بلورهای آنها,
محلول سازی
معمولا براي کار در آزمايشگاه از محلولهاي استاندارد استفاده ميکنند. محلولي را استاندارد مي گويند که در آن ، رابطه بين مقادير ماده حلشده و محلول يا رابطه بين مقدار ماده حلشده و حلال بنحوي معلوم باشد. با معلوم بودن مقدار ماده حلشونده و مقدار حلال تشکيل دهنده محلول ، غلظت محلول مشخص ميگردد. بسياري از واکنشها در حالت محلول انجام ميشوند و محاسبههاي کمي براي اينگونه واکنشها بر مبناي غلظت آنها صورت ميگيرد.
محلولي را استاندارد مي گويند که در آن ، رابطه بين مقادير ماده حلشده و محلول يا رابطه بين مقدار ماده حلشده و حلال بنحوي معلوم باشد. با معلوم بودن مقدار ماده حلشونده و مقدار حلال تشکيل دهنده محلول ، غلظت محلول مشخص ميگردد. بسياري از واکنشها در حالت محلول انجام ميشوند و محاسبههاي کمي براي اينگونه واکنشها بر مبناي غلظت آنها صورت ميگيرد. براي بيان غلظت ، روشهاي گوناگوني وجود دارد و محلولهاي استاندارد را براساس غلظت بيان ميکند.
محلولهاي استاندارد کاربردهاي زيادي دارند، از جمله در تجزيه هاي تيترسنجي (تيتراسيون) ، واکنشهاي خنثي شدن و واکنشهاي اکسيداسيون-احيا و...
محلولهای استاندارد کاربردهای زیادی دارند، از جمله در تجزیه های تیترسنجی (تیتراسیون) ، واکنشهای خنثی شدن و واکنشهای اکسیداسیون-احیا و...
این مطلب در تاریخ: یک شنبه 24 آذر 1392 ساعت: 5:48 منتشر شده است
برچسب ها : محلول سازی,
پلاریمتری
فعالیت نوری میزان توانایی یک ماده در چرخش نور قطبیده مسطح میباشد. اگر جسم شفافی بتواند سطح نوسان بردار میدان الکتریکی را به اندازه زاویه (آلفا) بچرخاند، میگویند جسم توانایی چرخش نور را داشته یا از نظر نوری فعال است. این پدیده اولین بار در سال 1811میلادی برای کوارتز گزارش شد و از آن به بعد مطالعات وسیعی در مورد آن انجام شده است. در اواسط قرن نوزدهم میلادی قوانین بنیادی در مورد فعالیت نوری وضع گردید که منجر به پیشرفت اساسی در شیمی فضایی ترکیبات آلی شد. امروزه برخی از همان نظریات مورد قبول است. در فعالیت نوری ، ماده و نور ، با واکنش متقابل سبب چرخش نور قطبیده مسطح میشوند.
محلولهای فعال نوری
محلولهای فعال نوری ، محلولهایی هستند که دارای کربن نامتقارن میباشند، مانند گلوکز ، اسید تارتاریک ، اسید لاکتیک. این محلولها قادرند صفحه پولاریزاسیون را بچرخانند که مقدار زاویه چرخش متناسب با غلظت مایع و طولی از آن میباشد که نور قطبیده از آن میگذرد. همچنین مقدار زاویه به طول موج نور تابشی بستگی دارد که معمولا از خط سدیم (5893 آنگستروم) استفاده میکنند. درجه حرارت و نوع حلال هم تا حدودی در این مقدار موثر هستند.
این مطلب در تاریخ: یک شنبه 24 آذر 1392 ساعت: 5:42 منتشر شده است
برچسب ها : پلاریمتری,










