اندازه گیری فشار خون در خانه نشان می دهد که در طول روز چقدر فشار خون تان تغییر می کند و پزشک شما از روی عددهایی که نوشته اید، پی به این نکته می برد که داروهای تان برای کنترل فشار خون بالای شما چه قدر موثر است. در واقع اندازه گیری فشار خون نوعی مدیریت سلامت بدن می باشد.
برای اندازه گیری فشار خون به چه وسایلی نیاز است؟
برای اندازه گیری فشار خون در خانه، می توانید از مونیتور آنروید(aneroid) یا مونیتور دیجیتالی بر حسب نیازتان استفاده کنید.
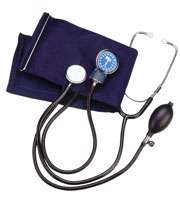
مونیتور آنروید، دارای اعداد و ارقامی است که با نگاه کردن به صفحه ی نمایشگر، کاملاً مشخص می شوند. این نوع از دستگاه های اندازه گیری فشار خون روی بازو بسته و بعد با دست باد می شوند(با باد کردن یک حباب پلاستیکی که به دستگاه وصل است).
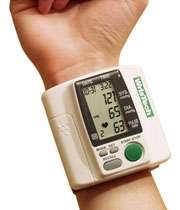
مونیتور دیجیتالی روی مچ دست بسته و میزان فشار خون روی یک صفحه کوچک نمایشگر، ثبت می شود.
مزایا و معایب مونیتورهای آنروید
مزیت اصلی مونیتورهای آنروید این است که به راحتی از جایی به جای دیگر منتقل می شوند. این نوع از فشار سنج ها معمولاً از فشار سنج هایی که مونیتور دیجیتالی دارند، ارزان تر هستند، اما کار کردن با آن ها کمی پیچیده است و به راحتی دچار اختلال شده و در این شرایط اعداد و ارقامی که نشان می دهند، دیگر دقیق و درست نیستند.
به علاوه ممکن است باد کردن حباب پلاستیکی کمی دشوار باشد در ضمن افرادی که ناشنوایی دارند، نمی توانند از مونیتور آنروید استفاده کنند؛ زیرا با گوشی ضربان سنج قادر به شنیدن صدای قلب نیستند.
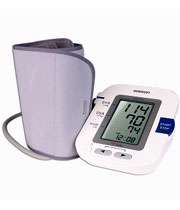
مزایا و معایب مونیتورهای دیجیتالی
از آن جایی که مونیتورهای دیجیتالی خودکار هستند، یکی از متداول ترین دستگاه ها برای اندازه گیری فشار خون محسوب می شوند.
با این دستگاه میزان فشار خون به راحتی خوانده می شود؛ زیرا اعداد روی یک صفحه، نمایش داده می شوند.
استفاده از آن ها به مراتب ساده تر از مونیتورهای آنروید است.
در ضمن افراد ناشنوا نیز به راحتی می توانند از آن استفاده کنند؛ زیرا نیاز به شنیدن صدای قلب از طریق گوشی نیست.
اما عیب اصلی این دستگاه ها این است که صحت و دقت اعداد با هر تکان بدن تغییر می کند و دیگر این که نیاز به باتری دارند.
برخی از انواع مونیتورهای دیجیتالی به نوعی طراحی شده اند که فقط برای دست چپ قابل استفاده هستند.
آیا می توان از مونیتورهای انگشتی برای اندازه گیری فشار خون استفاده کرد؟
تحقیقات نشان می دهند که مونیتورهای انگشتی دقت بالایی ندارند و ضریب خطا در آن ها کمی بیشتر است.
همچنین نسبت به تکان های بدن بسیار حساس هستند و البته در مقایسه با سایر دستگاه های فشار خون، قیمت بالاتری هم دارند.
ویژگی های مونیتور فشار خون
- مونیتور فشار خون از نوع مچ دست باید اندازه ای متناسب با مچ دست شما داشته باشد. به هنگام خرید حتماً از فروشنده ی متخصص بخواهید که با توجه به اندازه ی بازو و مچ دست تان مونیتور مناسب به شما بدهد.
- اعداد روی مونیتور باید به آسانی خوانده شوند.
- اگر از گوشی ضربان سنج استفاده می کنید، باید صدای قلب خود را با آن بشنوید.
- از آن جایی که دستگاه های فشار خون خانگی قیمت های متفاوتی دارند نسبت به مبلغی که پرداخت می کنید، حواس تان جمع باشد.
چطور می توان از کارکرد صحیح دستگاه مطمئن شد؟
وقتی که دستگاه را می خرید، بهتر است آن را به پزشک خود نیز نشان دهید تا نسبت به درستی آن اطمینان حاصل کنید.
هر سال یک بار مونیتور فشارسنج خود را چک کنید.
همواره از آن مراقبت کرده و از قرار دادن در محیط بسیار گرم خودداری کنید.
اگر مونیتور شما دارای تلمبه ی بادی است، مراقب باشید که دچار بریدگی و سوراخ شدگی نشود؛ برای اطمینان بیشتر می توانید از یک پزشک یا یک پرستار بخواهید که طریقه ی استفاده ی صحیح آن را به شما آموزش دهد.
با استفاده ی صحیح از وسیله ای که خریده اید، می توانید همواره فشارخون خود را کنترل کنید.
اطلاعاتی که روی مونیتورها نمایش داده می شوند:
فشار خون: نیروی خون که به دیواره رگ های خونی وارد می شود (Blood Pressure)
فشار خون بالا: (Hypertension)
فشار خون پایین: (Hypotension)
رگ های بازویی: رگ های خونی هستند که از شانه ها می آیند و تا پایین آرنج ادامه دارند و شما فشارخون را در این رگ ها اندازه گیری می کنید (Bracial artery).
فشار سیستولیک: بیشترین فشار در رگ های خونی است؛ یعنی وقتی که قلب مثل تلمبه، خون را به همه جای بدن می رساند.
فشار دیاستولیک: کمترین فشار در رگ های خونی؛ یعنی وقتی است که قلب در حال استراحت می باشد.
میزان فشار خون: منظور فشار سیستولیک و دیاستولیک است و معمولاً به این شکل نوشته می شود: (مثلا 80/120) بالاترین عدد مربوط به فشار سیستولیک اول می آید.
قبل از اندازه گیری فشار خون، باید چه کرد؟
- قبل از اندازه گیری فشار خون، (حدود 30 دقیقه قبل)، از مصرف کافئین، الکل، توتون و امثال این ها خودداری کنید.
- به دستشویی رفته و ادرار کنید.
- 3 تا 5 دقیقه در حالت استراحت قرار بگیرید و حرف نزنید تا اندازه دقیق تری به دست آید.
- در یک موقعیت راحت بنشینید، دست ها و پاهای تان را به هم نچسبانید.
- دست چپ خود را در راستای قلب تان دراز کنید یا روی میز بگذارید تا ثابت بماند.
- آستین لباس تان را بالا بزنید و دستگاه را به آرامی روی دست خود ببندید.
طریقه ی استفاده از مونتیورهای آنروید یا دستی
1- گوشی ضربان سنج را به گوش بزنید.
2- بازوبند را دور بازوی خود بپیچید؛ خیلی محکم و یا خیلی شل نباشد.
3- حباب پلاستیکی را با سرعت باد کنید(آرام باد کردن در صد خطا را افزایش می دهد)
4- به آرامی دریچه را شل کنید و اجازه دهید هوا کم کم از قسمت بازوبند دستگاه خارج شود و بعد آن را در هر ثانیه به اندازه ی 2 تا 3 میلی متر، باد کنید اگر مقدار باد خیلی زیاد باشد، نمی توانید رقم دقیق فشارخون را متوجه شوید.
5- به محض خروج هوا از بازوبند صدا ضربان قلب را خواهید شنید. به اولین صدای قلب خود توجه داشته باشید، آن عدد فشار سیستولیک را نشان می دهد.
6- باد کردن بازوبند را ادامه داده و به صدای ضربان قلب خود گوش دهید. برخی لحظات صدای ضربان قلب تان قطع می شود (حالت استراحت قلب) عددی که در این لحظات روی نمایشگر می بینید، فشار دیاستولیک شما را نشان می دهد.
7- اگر می خواهید اندازه گیری فشار خون را مجدداً تکرار کنید، 2 تا 3 دقیقه صبر کنید و بعد این کارها را دوباره انجام دهید.
طریقه ی استفاده از مونیتورهای دیجیتالی
1- دستگاه را به دور بازوی خود ببندید و دکمه روشن شدن دستگاه را فشار دهید تا شروع به کار کند.
2- دستگاه به طور خودکار باد می کند و شما فقط باید یک دکمه را فشار دهید. بعد از باد شدن، دستگاه به طور خودکار شروع به خارج کردن باد کرده و فشار روی دست کمتر و کمتر می شود.
3- با نگاه کردن به مونیتور دستگاه می توانید فشارخون خود را روی آن بخوانید. این دستگاه فشار سیستولیک و دیاستولیک شما را نیز روی صفحه نمایش می دهد.
4- دکمه اتمام کار(خروج) را بزنید تا تمام باد خارج شود.
5- در صورت تمایل به تکرار اندازه گیری 2 تا 3 دقیقه صبر کنید و بعد این مراحل را انجام دهید.
فشارخون طبیعی 80/120 یا کمی پایین تر و فشارخون بالا، 90/140 یا بالاتر است. اگر فشارخون شما بین 80/120 تا 90/140 باشد، وضعیت شما وضعیت قبل از فشارخون بالا است(Prehypertension) به این معنی که در مراحل نخست خطر بالا رفتن فشارخون هستید.
در افرادی که دیابت یا مشکلات کلیوی دارند، میزان فشارخون شان در مقایسه با افراد دیگر باید کمتر باشد.
فشارخون پایین نیز مربوط به زمانی است که فشار سیستولیک کمتر از 90 باشد. فشارخون بسیار پایین ایجاد شوک می کند و خطری بسیار جدی تلقی می شود.
ماهنامه ی دنیای سلامت
می پسندم 0 نمی پسندم 0
این مطلب در تاریخ: یک شنبه 24 فروردين 1393 ساعت: 18:40 منتشر شده است









 5- آستین بیمار را بالا بزنید و یا دست او را از داخل آستین لباس بیرون بیاورید. سپس در حالی که دست بیمار کمی خمیده است آن را طوری قرار دهید که کف دست به طرف بالا قرار گرفته و ساعد همسطح قلب قرار گیرد (چنانچه ساعد پایین تر از سطح قلب قرار گیرد فشار خون، بیشتر و چنانچه بالاتر از سطح قلب قرار گیرد فشار خون کمتر نشان داده خواهد شد).
5- آستین بیمار را بالا بزنید و یا دست او را از داخل آستین لباس بیرون بیاورید. سپس در حالی که دست بیمار کمی خمیده است آن را طوری قرار دهید که کف دست به طرف بالا قرار گرفته و ساعد همسطح قلب قرار گیرد (چنانچه ساعد پایین تر از سطح قلب قرار گیرد فشار خون، بیشتر و چنانچه بالاتر از سطح قلب قرار گیرد فشار خون کمتر نشان داده خواهد شد).















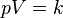
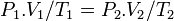
 فشار گاز ایدهآل در قبل از فرآیند
فشار گاز ایدهآل در قبل از فرآیند حجم گاز ایدهآل در قبل از فرآیند
حجم گاز ایدهآل در قبل از فرآیند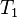 دمای گاز ایدهآل در قبل از فرآیند
دمای گاز ایدهآل در قبل از فرآیند فشار گاز ایدهآل در بعد از فرآیند
فشار گاز ایدهآل در بعد از فرآیند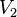 حجم گاز ایدهآل در بعد از فرآیند
حجم گاز ایدهآل در بعد از فرآیند دمای گاز ایدهآل در بعد از فرآیند
دمای گاز ایدهآل در بعد از فرآیند